运用元素周期律分析下面的推断,其中错误的是
| A.砹(At)为有色固体,HAt不稳定 |
| B.铊(T1)是铝的同族元素,原子核外有6个电子层,推测T1(OH)3是两性氢氧化物 |
| C.已知锶Sr与镁同族且原子半径大于钙,硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)比硫化氢稳定性差 |
某溶液中大量存在以下浓度的五种离子:0.2 mol/L Cl-、0.4 mol/L SO42-、0.1 mol/L Al3+、0.3 mol/L H+、M,则M及物质的量浓度可能为
| A.Na+ 0.3 mol/L | B.Zn2+ 0.2 mol/L | C.CO32- 0.2 mol/L | D.Ca2+ 0.1 mol/L |
下列实验操作正确的是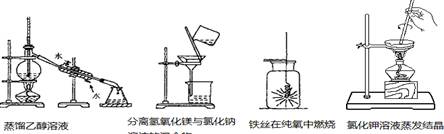
ABC D
在遇铁粉能产生大量气体的溶液中,可以大量共存的是
| A.K+、Cl-、NO、CH3COO- | B.Na+、Ca2+、Cl-、HCO |
| C.Na+、SO42-、NH4+、NO | D.Ba2+、K+、NO、SO42- |
下列离子方程式正确的是
| A.澄清石灰水与盐酸反应:H++OH-===H2O |
| B.醋酸溶液与碳酸钠溶液:CO32-+2H+===CO2↑+H2O |
| C.金属镁与稀盐酸反应:Mg+2H++2Cl-===MgCl2+H2↑ |
| D.氢氧化钡溶液与硫酸镁溶液反应:Mg2+ + 2OH- = Mg(OH)2↓ |
下列说法正确的是
| A.氨水能导电,所以氨水是电解质 |
| B.氯化银不能形成水溶液而导电,所以氯化银是非电解质 |
| C.液体硫酸虽然是电解质,但本身不导电 |
| D.电解质在任何条件下都导电,非电解质在任何条件下都不能导电 |