在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g) 2HBr(g);ΔH<0。当温度分别为T1、T2平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
2HBr(g);ΔH<0。当温度分别为T1、T2平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是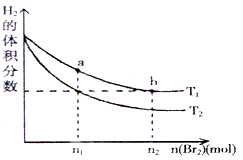
| A.由图可知:T2>T1 |
| B.两点的反应速率:a>b |
| C.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加 |
| D.a点比b点体系的颜色深 |
燃料电池是利用燃料(如H2、CO、CH4等)跟氧气或空气反应,将化学能转化成电能的装置,电解质溶液是强碱。下面关于甲烷燃料电池的说法正确的是
| A.负极反应为:O2+2H2O+4e ==4OH-; |
| B.负极反应为:CH4+10OH- - 8e==CO32-+7H2O |
| C.放电时溶液中的阳离子向负极移动; |
| D.随放电的进行,溶液的pH值不变 |
在0.10 mol·L—1CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO— +H+对于该平衡,下列叙述正确的是
CH3COO— +H+对于该平衡,下列叙述正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.10 mol·L—1HCl溶液,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
已知下列热化学方程式:
(1) H2(g)+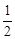 O2(g)= H2O(g);ΔH1=" a" kJ/mol
O2(g)= H2O(g);ΔH1=" a" kJ/mol
(2) 2H2(g)+O2(g)=2H2O(g);ΔH2=" b" kJ/mol
(3) H2(g)+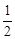 O2(g)=H2O(l);ΔH3=" c" kJ/mol
O2(g)=H2O(l);ΔH3=" c" kJ/mol
(4) 2H2(g)+O2(g)=2H2O(l);ΔH4=" d" kJ/mol
下列关系式正确的是
| A.a<c<0 | B.b>d>0 | C.2c=b>0 | D.2c=d<0 |
下列与化学反应能量变化相关的叙述正确的是
| A.生成物能量一定低于反应物总能量 |
| B.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 |
| C.根据盖斯定律,可计算某些难以直接测定的化学反应的反应焓变 |
D.同温同压下,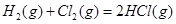 在光照和点燃条件的 在光照和点燃条件的 不同 不同 |
用0.1mol·L—1的盐酸滴定0.1mol·L—1的氨水,在滴定过程中不可能出现的结果是
| A.c(NH4+)>c(Cl-),c(OH-)>c(H+) |
| B.c(NH4+)=c(Cl-),c(OH-)=c(H+) |
| C.c(Cl-)>c(NH4+),c(OH-)>c(H+) |
| D.c(Cl-)>c(NH4+),c(H+)>c(OH-) |