下图为中学化学中几种常见物质之间的转化关系。
已知:
①A、C、D是常见的气体单质;
②F气体极易溶于水,且液态常用做制冷剂;
③G为易溶性的盐,E为白色沉淀;
④H为无色液体化合物。
(1)写出D的原子结构示意图 。
(2)鉴定G中阳离子的实验方法和现象
。
(3)反应②的离子方程式 。
(4)反应③的化学方程式 。
(5)将等物质的量的F与G溶于水,所得溶液pH>7,则该溶液中各种离子浓度大小顺序为 。
下一代iPhone将在电池方面有所改进,该电池的一极为一种有机高分子游离基(用R表示)和石墨粉及粘结剂的复合材料,另一极是锂,分隔材料为某种聚烯烃,电解质为LiPF6溶解于某种有机碳酸酯溶剂中。该游离基(R)在空气中十分稳定,在充电时被氧化成阳离子(Rx+),电池充放电的方程式为:xLi+Rx+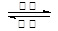 xLi++R。下列有关说法正确的是
xLi++R。下列有关说法正确的是
| A.放电时,该电池将电能转化为化学能 | B.充电时,Rx+由阴极向阳极移动 |
| C.放电时,负极反应为xLi-xe-==xLi+ | D.充电时,阳极反应为R-xe-==Rx+ |
用下列实验装置进行相应的实验,能达到实验目的的是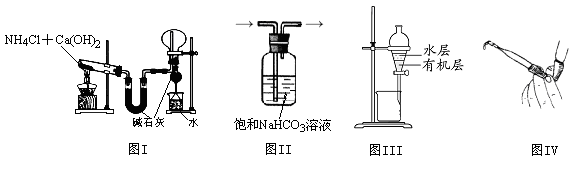
| A.图I用于实验室制氨气并收集干燥的氨气 | B.图II用于除去CO2中含有的少量HCl |
| C.图III用于提取I2的CCl4溶液中的I2 | D.图IV用于检查碱式滴定管是否漏液 |
有A、B、C、D、E五种短周期元素,A是地壳中含量最多的元素,B元素有3种同位素B1、B2、B3,B3原子的质量数是B1的3倍,C是非金属性最强的元素,D和C可以形成DC型离子化合物,且离子的电子层结构相同,E元素原子的最外层电子数比内层电子总数少6个。下列说法正确的是
A.D元素的金属性在短周期元素中最强
B.E单质常用作半导体材料和光导纤维
C.A和B只能形成原子个数比1︰2的化合物
D.以上元素中形成的最高价氧化物对应的水化物酸性最强的是C
下列各组离子能大量共存的是
| A.NaClO水溶液中:Fe2+、Cl-、Ca2+、H+ |
| B.加入KSCN显红色的溶液:K+、Na+、I-、S2- |
| C.无色酸性溶液中:K+、CH3COO-、HCO3-、MnO4- |
| D.pH=2的溶液中:NH4+、Na+、Cl-、Cu2+ |
叠氮酸钠(NaN3)是无色离子晶体,遇高温或剧烈震动能发生强烈爆炸,快速分解成钠单质和氮气,是汽车安全气囊中的成分之一。下列有关说法正确的是
| A.NaN3中只含有离子键 |
| B.1molNaN3完全分解最多可以产生33.6LN2 |
| C.NaN3快速分解时,NaN3既是氧化剂,又是还原剂 |
| D.常温下,NaN3化学性质稳定,包装盒上无需特别说明注意事项 |