下列叙述中正确的是
| A.已知反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O,其中1mol氧化剂得到11mole- |
| B.向NaClO溶液中通入少量SO2的离子方程式为:ClO-+SO2+H2O=Cl-+SO42-+2H+ |
| C.已知反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,该反应中Cu2S既是氧化产物又是还原产物 |
| D.某反应体系中的物质有:N2O、FeSO4、Fe2(SO4)3、HNO3、Fe(NO3)3、H2O,若H2O是生成物,则N2O是还原产物 |
甲乙丙是三种不含相同离子的可溶性电解质。他们所含的离子如表所示。取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)<c(乙)<c(丙),下列说法正确的是
| 阳离子 |
Na+ NH4+ Fe3+ |
| 阴离子 |
OH- Cl- SO42- |
A、甲中一定含有Na+ B、乙中一定含有NH4+
C、丙中一定含有 Fe3+ D、丙中一定含有SO42-
设NA为阿伏伽德罗常数的值,下列说法正确的是
A.1 mol 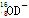 离子含有的质子、中子数均为10NA 离子含有的质子、中子数均为10NA |
| B.标准状况下,4.48 L己烷含有的分子数为0.2NA |
| C.含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA |
| D.VL a mol•L﹣1的氯化铁溶液中,若Fe3+的数目为NA,则Cl﹣的数目等于3NA |
下列说法不正确的是
| A.甲装置可以用于比较Fe3+ 、I2 、Cl2的氧化性强弱 |
| B.乙装置中橡皮管的作用是使水能顺利流下 |
| C.丙装置中,若向Ba(OH)2溶液中逐滴加入硫酸溶液直至过量,灯光会由亮变暗至熄灭后又逐渐变亮 |
| D.丁装置用于吸收HCl气体能防倒吸 |
成语“恶狗酒酸”中隐藏着一个寓言故事:人有市酒而甚美者,然至酒酸而不售,问里人其故。里人曰:公之狗甚狂,人有持器往者,狗辄迎面啮之,是以酒酸不售也。 下列关于“酒”的说法错误的是
| A.“恶狗酒酸”的成语中涉及了氧化反应 |
| B.糖类、油脂都可以用来酿酒 |
| C.葡萄糖转变成酒精的过程放出热量 |
| D.工业酒精中因含有剧毒物质甲醇而不能用来勾兑饮用酒水 |
已知25℃下碳酸的电离常数K1=4.4×10-7,K2=4.7×10-11。下列有关碳酸溶液中各微粒浓度关系的说法正确的是
A. |
B. |
C.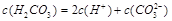 |
D. |