核电是一种高效能源,也是一种高危能源。例如会泄露出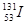 ,当达一定浓度时,会对人体有伤害。
,当达一定浓度时,会对人体有伤害。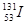 中质子数比中子数少:
中质子数比中子数少:
| A.131 | B.53 | C.25 | D.78 |
下列叙述中错误的是 ( )
| A.相同体积的任何气体都含有相同数目的分子。 |
| B.标准状况下,5L H2S气体与5L NH3的原子个数比为3∶4。 |
| C.同温同压下相同体积的N2气和CO气体含有相同物质的量、相同的质量和相同的对空气的密度。 |
| D.相同温度下,气体的压强比等于气体体积的反比。 |
某钠盐溶液中可能含有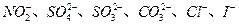 等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中只含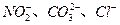 三种阴离子。
三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
| A.①②④⑤ | B.③④ | C.③④⑤ | D.②③⑤ |
下列热化学方程式或离子方程式中,正确的是:
| A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:有CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1 |
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: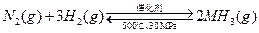 △H=-38.6kJ· △H=-38.6kJ· mol-1 mol-1 |
C.氯化镁溶液与氨水反应: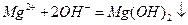 |
D.氧化铝溶于NaOH溶液: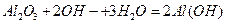 |
将质量分数为0.052(5.2%)的NaOH溶液1 L(密度为1.06 g/cm3),用铂作电极电解,当溶液中NaOH的质量分数改变了0.010(1.0%)时停止电解,此时溶液中符合下表关系的是( )
| NaOH的 质量分数 |
阳极析出 物质的质量/g |
阴极析出物 质的质量/g |
|
| A |
0.062(6.2%) |
19 |
152 |
| B |
0.062(6.2%) |
152 |
19 |
| C |
0.042(4.2%) |
1.2 |
9.4 |
| D |
0.042(4.2%) |
9.4 |
1.2 |
已知H2(g)+Br2(l)="2HBr(g)" △H="-72kJ/mol." 蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
则表中a为
| A.404 | B.260 | C.230 | D.200 |