(12分) 诺贝尔物理学奖曾授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
(1)在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。
则分子中B原子杂化轨道的类型为 ▲ ,同层分子间的主要作用为 ▲ 。
(2)K3[Fe(CN)6]晶体 中含有的化学键类型为 ▲ ,Fe3+与CN-之间能够形成化学键的原因是 ▲ 。
中含有的化学键类型为 ▲ ,Fe3+与CN-之间能够形成化学键的原因是 ▲ 。
(3)等物质的量的氧化物MO与SiC的电子总数相等,则M2+离子的核外电子排布式为 ▲ 。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似,晶体中与每个M2+等距离且最近的几个O2-所围成的空间几何构型为 ▲ 。MO的熔点比CaO的高,原因是 ▲ 。
(8分,每空格2分)常温下,0.1m01/L的下列溶液:
①HCl、②CH3COOH、③CH3COONa、④NaOH、⑤FeCl3、⑥NaCl。
(1)pH由小到大排列顺序为(填序号);
(2)实验室配制⑤的溶液时常需加入少量盐酸,否则得到的是浑浊的溶液,产生浑浊的原因是(用离子方程式表示)
(3)物质的量浓度相同的①氨水②氯化铵③碳酸氢铵④硫酸氢铵⑤硫酸铵
在上述五种溶液中,铵根离子物质的量浓度由大到小的顺序是
(4)已知拆开1molH—H键,1molN—H键,1molN≡N键分别需要的能量是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(10分,每空格2分)原子结构与元素周期表存在着内在联系。请回答下列问题:
(1)具有(n-1)d10ns电子构型的元素位于周期表中区。
(2)被誉为“21世纪金属”的钛(Ti)元素原子的价电子排布式为:。
(3)写出地壳中含量最多的金属元素原子的核外电子排布式。
(4)写出3p轨道上有2个未成对电子的元素的符号:。
(5)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一为绿色。两种晶体的组成都为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:a分别取等质量的两种配合物晶体的样品配成待测溶液;b分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;c沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的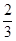 。该绿色晶体配合物的化学式为
。该绿色晶体配合物的化学式为
A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体。而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。请回答下列问题:
(1)写出A、B、C、D、E、F的化学式
A、 ______B、 _____C、 _____D、 ___E、 __F、。
(2)写出F和H反应的化学方程式。
(3)写出下列反应的离子方程式:
① D+盐酸。
② B+水。
(1)现有73g某双原子分子气体,它的摩尔质量为36.5 g·mol—1。则:
① 该气体的物质的量为mol。
② 该气体所含原子数为NA。
③ 该气体在标况下的体积为L。
④该气体完全溶于500mL水后稀释到2L,物质的量浓度为mol·L—1。
(2)将100mL 0.5mol/L Na2SO4溶液加水稀释到500mL,稀释后:c(Na+)=mol·L—1。
(3)g H2O中的O原子数目与标准状况下2.24LCO2中的O原子数目相同。
物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看做是化学平衡的一种。请根据所学化学知识回答下列问题:
Ⅰ、已知0.01mol/L的NaHCO3溶液呈碱性。
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示:
①②③。
(2)溶液中共有种不同的粒子(指分子和离子)。
(3)该溶液中的离子浓度由大到小的顺序是:。
(4)向该溶液中加入AlCl3溶液,有白色胶状沉淀生成,同时产生一种无色无味并能使澄清石灰水变浑浊的气体,写出该反应的离子方程式:。