下列离子方程式书写正确的是
A.实验室用大理石和稀盐酸制取CO2: 2H++CO =CO2↑+H2O =CO2↑+H2O |
| B.铁和稀硝酸反应:Fe+2H+===H2↑+Fe2+ |
| C.向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH- =Al(OH)3↓ |
D.用氢氧化钠检验氯化铵溶液中铵根离子:NH4++OH- NH3↑+H2O NH3↑+H2O |
将4.48g Fe溶于1L 0.2mol·L-1的稀硫酸,再加入50mL 0.4mo1·L-1KNO3溶液后,其中的Fe2+全部转化成Fe3+,NO3-无剩余,生成一种氮氧化物NYOX。则该氮氧化物的化学式是
| A.N2O | B.NO | C.N2O3 | D.NO2 |
根据下图,下列判断正确的是
| A.电子从Zn极流出,流入Fe极,经盐桥回到Zn极 |
| B.烧杯a中发生反应O2+4H++4e-=2H2O,溶液pH升高 |
| C.烧杯b中发生的电极反应为Zn-2e-=Zn2+ |
| D.向烧杯a中加入少量K3Fe(CN)6溶液,有蓝色沉淀生成 |
下列表格中的各种情况,可以用下图的曲线表示的是
| 反应 |
纵坐标 |
甲 |
乙 |
|
| A |
相同质量的氨,在同一容器中2NH3   N2 + 3H2ΔH<0 N2 + 3H2ΔH<0 |
氨气的转化率 |
500℃ |
400℃ |
| B |
等质量等颗粒大小的钾、钠分别与足量水反应 |
H2质量 |
钠 |
钾 |
| C |
在体积可变的恒压容器中,体积比1︰3的N2、H2,N2 + 3H2  2NH3 2NH3 |
氨气的浓度 |
活性高的催化剂 |
活性一般的催化剂 |
| D |
2 molSO2和1 molO2,在相同温度下 2SO2 + O2  2SO3 2SO3 |
SO3物质的量 |
2个大气压 |
10个大气压 |
下列说法错误的是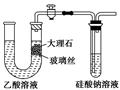
| A.使用如图所示装置验证Ka(CH3COOH)>Ka(H2CO3)>Ka(H2SiO3) |
| B.0.1 mol·L-1的醋酸中加入水或加入冰醋酸均可使醋酸电离平衡向电离方向移动 |
| C.等物质的量浓度的CH3COONa和Na2CO3溶液,后者溶液中水的电离程度大 |
| D.等pH的醋酸和碳酸,分别加水稀释后溶液的pH仍相等,则醋酸中加入水的体积少 |
下列各组离子,能在指定溶液中大量共存的是
①无色溶液中:K+、Cl-、Na+、HCO3-、OH-
②使甲基橙变红的溶液中:MnO4-、NO3-、SO42-、Na+、Fe3+
③水电离的c(H+)=10-12mol·L-1的溶液中:ClO-、HCO3-、NO3-、NH4+
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、Na+、SO42-
⑤使pH试纸变深蓝色的溶液中: K+、CO32-、Na+、AlO2-
⑥pH=0的溶液中:Fe2+、Al3+、NO3-、Cl-、SO32-
| A.①②③ | B.②④⑤ | C.①②⑤ | D.③⑤⑥ |