6.4g铜与过量的硝酸(8mol / L,60mL)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+为 n mol,此时溶液中所含NO3–物质的量为
| A.0.28mol | B.0.31mol |
| C.(n + 0.2) mol | D.(n + 0.4) mol |
下列推断合理的是
| A.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| B.金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
| C.浓H2SO4有强氧化性,不能与Cu发生剧烈反应 |
| D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
利用下列实验装置完成相应的实验,能达到实验目的的是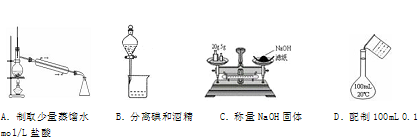
某混合溶液中所含离子的浓度如下表,则M n+离子及a值可能为
| 所含离子 |
NO3– |
SO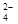 |
H+ |
Na+ |
M n+ |
| 浓度(mol / L) |
3 |
1 |
2 |
1 |
a |
A.Fe2+、2 B.Ba2+、0.5 C.Al3+、1.5 D.Mg2+、1
化学实验中,常将溶液或试剂进行酸化,下列试剂选择和酸化处理正确的是
A.定性检验SO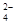 ,将BaCl2溶液用HNO3酸化 ,将BaCl2溶液用HNO3酸化 |
| B.为了提高KMnO4溶液的氧化能力,用盐酸将其酸化 |
| C.检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液 |
| D.配制FeCl2溶液时通常加少量HNO3酸化,以避免其变质 |