吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”,科学家尝试用Na2SeO3消除人体内活性氧,则Na2SeO3的作用是
| A.氧化剂 | B.还原剂 | C.既是氧化剂又是还原剂 | D.以上均不是 |
下列电子式正确的是()
A.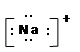 |
B.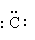 |
C.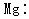 |
D.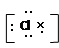 |
1mol/L的Na2SO4溶液是()
| A.溶液中含有1mol Na2SO4 |
| B.1升水中加入142g Na2SO4 |
| C.1mol Na2SO4溶于1mol水中 |
| D.将322g Na2SO4·10H2O溶于少量水后再稀释成1000mL |
已知a克N2含有b个分子,则阿伏加德罗常数的数值为()
A. |
B. |
C. |
D. |
元素X的原子获得3个电子与元素Y的原子失去2个电子后,它们的电子层结构与氖原子的电子层结构相同。X、Y两种元素的单质在高温下反应得到的化合物的正确化学式为( )
| A.X2Y3 | B.Y3X2 | C.Y2X3 | D.X3Y2 |
在标准状况下,一氧化碳和二氧化碳的混合气体5.6L,如果一氧化碳的质量为5.6g,则二氧化碳的质量为( )
| A.5.6g | B.4.4 g | C.2.2g | D.1g |