下列每组的三种物质中,两边的固体均有导线连接,插入中间的液体中,其中能组成原电池的是
| A.Zn | H2SO4(稀) | C | B.Cu | 酒精 | Ag |
| C.Zn | CCl4 | Cu | D.Fe | H2SO4(稀) |  Fe Fe |
如图所示是一系列含硫化合物的转化关系(反应中生成的水已略去),其中说法正确的是()
| A.反应①说明SO2具有漂白性,反应②说明SO2具有酸性 |
| B.反应②中生成物n(Na2SO3):n(NaHSO3)=1:1时,则反应物n(SO2):n(NaOH)=1:2 |
| C.反应③④⑤均属于氧化还原反应 |
| D.工业上可利用反应②和反应④回收SO2 |
下列说法正确的是()
| A.电解、电镀、电化学腐蚀都需要通电才可进行 |
| B.Al、Fe、Cu三者对应的氧化物均为碱性氧化物 |
| C.浓H2SO4和新制氯水分别滴在pH试纸上均会出现先变红后褪色的现象 |
| D.从石油中得到汽油,可采用分馏的方法 |
下列说法正确的是()
| A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 |
| C.氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接存放在铝制容器中 |
| D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
在稀硫酸、纯碱、烧碱、小苏打、氧化铝、氧化铁、一氧化碳、二氧化碳、铝粉、铁片和木炭粉11种物质中,选择适当的物质确定下图中的5种物质,使连线的两种物质能发生反应。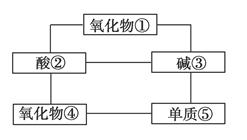
(1)写出它们的化学式:
①________,②________,③________,④________,⑤________。
(2)写出氧化物④与单质⑤反应的化学方程式_____________________________________
下列有关物质性质的描述和该性质的应用均正确的是( )
| A.氨气具有氧化性,用浓氨水检验氯气管道是否泄漏 |
| B.氢氟酸具有强酸性,用氢氟酸蚀刻玻璃 |
| C.二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气 |
| D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |