有反应K2S+2FeCl3 ===2FeCl2+2KCl+S试设计一原电池;画出示意图(仪器、溶液选择有烧杯、FeCl3溶液, FeCl3溶液,K2S溶液,导线,KCl盐桥,石墨电极,小灯泡,导线等材料)标明所选溶液,电极;写出电极反应;
负极;
正极;
画出示意图;
熔融盐燃料电池具有较高的发电效率,因而受到重视。某燃料电池以熔融的K2CO3(其不含O2-和HCO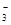 )为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。
)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。
该燃料电池负极电极反应式为:2C4H10+26CO -52e-=34CO2+10H2O。
-52e-=34CO2+10H2O。
试回答下列问题:
(1)该燃料电池的化学反应方程式为________________________________________________;
(2)正极电极反应式为_________________________________________。
(3)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此,必须在通入的空气中加入一种物质,加入的物质是________,它来自________________________________。
(4)某学生想用该燃料电池和如图所示装置来电解饱和食盐水:
①写出该电解池反应的离子方程式_______________________________________。
②将湿润的淀粉KI试纸放在该装置附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5∶1,且生成两种酸。该反应的化学方程式为___________________________________________________________。
③若电解后得到200 mL 3.25mol/LNaOH溶液,则消耗C4H10的体积在标准状况下为________mL。
X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
| 元素 |
相 关 信 息 |
| X |
X的基态原子L层电子数是K层电子数的2倍 |
| Y |
Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z |
Z的一种核素的中子数为12,质量数为23 |
| W |
W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)W位于元素周期表第____周期第____族,
基态W2+的核外电子排布式为。
(2)X的电负性比Y的____________(填“大”或“小”);X 和Y形成的XY32-离子中,中心原子的杂化类型是___________,其离子的空间构型为为。
(3)写出Z2Y2的电子式,指出其中含有的化学键;XY2形成的晶体类型为。
下图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出。已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于饮水消毒。反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法。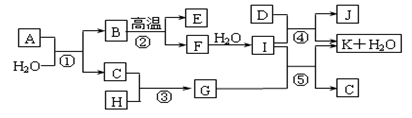
请回答下列问题:
(1)用电子式表示H的形成过程____________________;
(2)写出E溶液与过量I溶液反应的离子方程式______________________________。
(3)实验室还可用C的浓溶液与F制备气体C,反应理由是__________________________________________________。
(4)物质A由三种元素组成,1molA与水反应可生成1molB和2molC,A化学式为__________。
已知尿素的结构式为: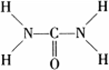 尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
(1)C、N、O三种元素的第一电离能由大到小的顺序是__________;电负性由大到小顺序是__________。
(2)尿素分子中C和N原子的杂化方式分别是__________、__________。
(3)NH4+中H—N—H键角比NH3中H—N—H键角大,原因为__________________________________________________。
(4)美国科学家合成了结构呈“V”形的N5+,已知该离子中各原子均达到8电子稳定结构。则有关该离子的下列说法中正确的是__________。
A.每个N5+中含有35个质子和36个电子
B.该离子中有非极性键和配位键
C.该离子中含有2个π键
D.与PCl4+互为等电子体
(5)[Fe(H2NCONH2)6](NO3)3中H2NCONH2与Fe(Ⅲ)之间的作用力是__________。FeCl3溶液与KSCN溶液混合,得到含多种配合物的红色溶液,其中配位数为5的配合物的化学式是__________。KSCN中的阴离子与CO2互为等电子体,该阴离子的电子式是__________。
A.B.C.D.E.F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A可形成分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期中简单离子半径最小的元素;基态E原子p能级上有一对成对电子,C.F两种元素的原子最外层共有13个电子。回答下列问题:
(1)D.E.F中电负性最大的是_______(填写元素符号)。
(2)写出D原子的外围电子排图为_______。
(3)B.C.E分别与A形成的化合物中沸点最高的是_______。
(4)C与D形成的化合物的化学式是_______,请写出其溶于NaOH的离子方程式_________________________;
(5)F的单质在反应中常作剂,该单质的水溶液与E的低价氧化物反应的离子方程式为_________________________。