如右图所示,常温,U形管内盛有100mL的某种溶液,
请按要求回答下列问题。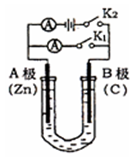
(1)若所盛溶液为CuSO4溶液,打开K2,合并K1,则:
① A为 极,B极的电极反应式为 。
②反应过程中,溶液中SO42-和OH-离子向 极(填:A或B)
移动。
(2)若所盛溶液为滴有酚酞的NaCl溶液,打开K1,合并K2,则:
①A电极可观察到的现象是 。
②电解过程总反应的化学方程式是 。
③反应一段时间后打开K2 ,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(折算成标准状况)为11.2mL,将溶液充分混合,溶液的pH为 。
④向电解后的电解质溶液中加入或通入 (填试剂名称),能使溶液复原。
气体X可能由NH3、Cl2、HBr、CO2中的一种或几种组成,已知X通入AgNO3溶液时产生浅黄色沉淀,该沉淀不溶于稀HNO3溶液,若将X通入澄清石灰水中,却不见沉淀产生,则有关气体X的成分的下列说法正确的是
①一定含有HBr,可能含有CO2 ②一定不含CO2 ③一定不含NH3、Cl2 ④可能含有Cl2、CO2
| A.只有① | B.只有③ |
| C.①和③ | D.②和③ |
下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)
| A.图1:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 |
| B.图2:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐 |
| C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 |
| D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |

现将等物质的量的CuSO4、FeCl3、Zn放入盛有水的烧杯中充分反应,所得溶液中除SO42-、Cl-外,还含有的金属阳离子是
| A.Zn2+、Cu2+、Fe3+ | B.Zn2+、Cu2+、Fe2+ |
| C.Zn2+、Fe2+、Cu2+、Fe3+ | D.Zn2+、Fe3+ |
酸根RO3-所含电子数比硝酸根NO3-的电子数多10,则下列说法正确的是
| A.R和N元素的原子含有相同数目的未成对电子 |
| B.RO3-中R的化合价与NO3-中的N的化合价不相等 |
| C.RO3-和NO3-只能被还原,不能被氧化 |
| D.R原子的电子层数比N的电子层数多1 |
取相同体积的KI、Na2S、FeBr2溶液,分别通入足量氯气,当反应恰好完成时三种溶液消耗氯气的体积相同(同温,同压条件下)。则KI、Na2S、FeBr2溶液的物质的量浓度之比为
A 6:3:2 B 1:2:3 C 3:6:2 D 2:1:3