对于可逆反应N2(g)+3H2(g)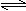 2NH3(g);△H<0,下列研究目的和示意图相符的是( )
2NH3(g);△H<0,下列研究目的和示意图相符的是( )
| |
A |
B |
C |
D |
| 研究 目的 |
压强对反应的影响(P2>P1) |
温度对反应的影响 |
平衡体系增加N2的浓度对反应的影响 |
催化剂对反应的影响 |
| 图示 |
 |
 |
 |
 |
工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)===Si(s)+4HCl(g)ΔH=+Q kJ·mol-1(Q>0)
某温度、压强下,将一定量的反应物通入密闭容器中进行以上反应(此条件下为可逆反应),下列叙述正确的是
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ |
| C.反应至4 min时若HCl浓度为0.12 mol·L-1,则H2反应速率为0.03 mol·L-1·min-1 |
| D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液中恰好反应 |
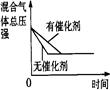
汽车尾气净化中的一个反应如下:
NO(g)+CO(g)
 N2(g)+CO2 (g)ΔH=-373.4 kJ·mol-1
N2(g)+CO2 (g)ΔH=-373.4 kJ·mol-1
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是

已知反应mX(g)+nY(g) qZ(g)的ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g)的ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
| A.通入稀有气体使压强增大,平衡将正向移动 |
| B.X的正反应速率是Y的逆反应速率的m/n倍 |
| C.降低温度,混合气体的平均相对分子质量变小 |
| D.增加X的物质的量,Y的转化率降低 |
如图所示是温度和压强对X+Y 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是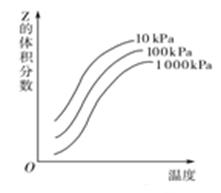
| A.上述可逆反应的正反应为放热反应 |
| B.X、Y、Z均为气态 |
| C.X和Y中只有一种为气态、Z为气态 |
| D.上述反应的逆反应的ΔH>0 |
1000 K时反应 C(s)+2H2(g) CH4(g)的K=0.5,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述反应
CH4(g)的K=0.5,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述反应
| A.正向移动 | B.逆向移动 | C.达到平衡 | D.不一定 |