下列离子方程式书写正确的是( )
A.溴乙烷与6mol/L的氢氧化钠水溶液共热:C2H5Br+OH-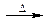 CH2=CH2↑+Br-+H2O CH2=CH2↑+Br-+H2O |
| B.等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合: Ca2++2HCO3  -+2OH- -+2OH- CaCO3↓+CO32-+2H2O[ CaCO3↓+CO32-+2H2O[ |
| C.在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入1~2滴盐酸: 3Fe2++4H++NO3-  3Fe3++NO↑+2H2O 3Fe3++NO↑+2H2O |
D.在H2O2中加入酸性高锰酸钾溶液:2MnO4-+6H++5H2O2 2Mn2++5O2↑+8H2O 2Mn2++5O2↑+8H2O |
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
| A.4Fe(OH)2+2H2O+O2=4Fe(OH)3↓ | B.2Fe+2H2O+O2=2Fe(OH)2↓ |
| C.2H2O+O2+4e-=4OH- | D.Fe-3e-=Fe3+ |
常温下某溶液中,由水电离出的[H+]为1×10—12mol/L,该溶液中一定能大量共存的离子组是
| A.K+、Na+、SO42—、NO3— | B.Na+、K+、S2—、CO32— |
| C.Fe2+、Mg2+、Cl—、SO42— | D.NH4+、Cl—、K+、SO32— |
下列混合溶液的pH一定小于7的是
| A.pH=3的盐酸和pH=11的氨水等体积混合 |
| B.pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
| C.pH=3的醋酸和pH=11的的氢氧化钡溶液等体积混合 |
| D.pH=3的硫酸和pH=11的氨水等体积混合 |
相同材质的铁在下图中各情形下最不易被腐蚀的是
X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为
| A.X>Z>Y>M | B.X>Y>Z>M | C.M>Z>X>Y | D.X>Z>M>Y |