氢氧燃料电池已用于航天飞机。以30% KOH溶液为电解质溶液的这种电池在使用时的电极反应如下: 2H2+4OH--4e- = 4H2O O2+2H2O+4e- = 4OH- 下列说法错误的是
| A.氧气通入正极发生氧化反应 |
| B.燃料电池的能量转化率不能达到100% |
| C.供电时的总反应为:2H2+O2 = 2H2O |
| D.产物为无污染的水,属于环境友好电池 |
将5 mL下列物质分别注入15 mL水中,振荡后静置,能形成如图所示分层现象的有 
①溴苯②乙酸乙酯③乙醇④甘油⑤油酸甘油酯⑥硝基苯
| A.全部 | B.①②⑤⑥ | C.②⑤ | D.①⑥ |
分子式为C5H9O2Cl,属于卤代酯且能发生银镜反应的同分异构体共有
| A.10种 | B.11种 | C.12种 | D.13种 |
短周期金属元素A和非金属元素B,它们的简单离子为aAm+和bBn-,已知bBn-比aAm+多两个电子层,则a的取值可以是:①1 ②2 ③3 ④4 ⑤5
| A.①② | B.③④ | C.①④ | D.③⑤ |
有关反应5Cu + 4H2SO4(浓) Cu2S + 3CuSO4 + 4H2O的叙述正确的是
Cu2S + 3CuSO4 + 4H2O的叙述正确的是
| A.氧化剂与还原剂的物质的量之比为1:5 |
| B.每有1 mol Cu参加反应时转移2 mol e- |
| C.氧化产物只有CuSO4 |
| D.浓硫酸既是氧化剂又是还原剂 |
下列物质互为同分异构体的一组是
| A.35Cl和37 Cl | B.CH3COOH和H—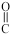 —OCH3 —OCH3 |
| C.O2和O3 | D.CH2=CH2和CH2—CH2 |