氢化铵(NH4H)与氯化铵结构相似,又已知NH4H 与水反应有H2生成,下列叙述中正确的是
| A.NH4H是共价化合物 | B.NH4H溶于水后,所形成的溶液显酸性 |
| C.NH4H溶于水时,NH4H是氧化剂 | D.NH4H固体投入少量水中,有两种气体生成 |
[化学--修3:物质结构与性质](15分)黄血盐(亚铁氰化钾,K4[Fe(CN)6] )易溶于水,广泛用做食盐添加剂(抗结剂),食盐中黄血盐的最大使用量为10 mg·kg-1。黄血盐经长时间火炒,超过400℃时会分解生成剧毒的氰化钾。回答下列问题:
(1)写出基态Fe2+的核外电子排布式________________________。K4[Fe(CN)6]中Fe2+与CN-两种离子之间的作用力是________________________。
(2)CN-中碳原子的杂化方式为____________;1molCN-中含有π键的数目为________。
(3)金属钾、铜的晶体的晶胞结构如下图(请先判断对应的图),钾、铜两种晶体晶胞中金属原子的配位数之比为________________________。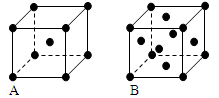
(4)黄血盐溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与CN-是等电子体的气态化合物,反应化学方程式为____________________________________________。
某温度下,将0.2 molC(S)和0.3 mol H2O(g)投入2L的密闭容器中,发生反应C(S)+H2O(g) CO + H25min达到平衡后,密度增加了0.3g/L。有关下列说法正确的是()
CO + H25min达到平衡后,密度增加了0.3g/L。有关下列说法正确的是()
| A.从反应开始到平衡过程中,用C来表示该反应的平均速率为0.005 mol•L-1•min-1 |
| B.达平衡时压强变为原来的7/6 |
| C.此温度下该反应的平衡常数为0.0125 |
| D.若保持温度和体积不变,向平衡体系中再加入0.2 molC(S)和0.3 mol H2O(g),重新达到平衡后,H2O的转化率等于16.7% |
下列叙述中不正确的是()
A.0.1 mol·L-1 NH4HS溶液中有: c(NH4+)<c(HS-)+c(S2-)+c(H2S)
B.某酸式盐NaHA溶液中一定有:c(OH-)+c(A2-)=c(H+) +c(H2A)
C.等浓度的HCN和NaCN混合溶液中有:2c(Na+)=c(CN—) + c(HCN)
D.等pH值的①(NH4)2SO4溶液②NH4HSO4溶液③NH4Cl溶液中,c(NH4+)的大小关系:①=③>②
有M、X、Y、Z、W五种原子序数依次增大的短周期元素,其中M、Z同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法正确的是
| A.X、M两种元素形成的化合物只能存在离子键 |
| B.元素Y、Z、W形成的单质中,每1mol它们的单质均含有NA个分子 |
| C.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
| D.元素W和M的某些单质可作为水处理中的消毒剂 |
下列离子方程式不正确的是 ()
| A.澄清石灰水与过量苏打溶液混合:Ca2++2OH-+2HCO3-=CaCO3↓ +CO32-+2H2O |
| B.用惰性电极电解NaHS溶液:HS-+ H2O电解S↓+H2↑+OH- |
| C.向摩尔盐溶液中加入过量的Ba(OH)2溶液: 2NH4+ + Fe2+ + 2SO42- + 2Ba2+ + 4OH- =2BaSO4↓+ Fe(OH)2↓+ 2NH3·H2O |
| D.明矾溶液中加入Ba(OH)2溶液至生成的沉淀质量最多: |
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O