酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是()
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧化合物
| A.②④ | B.②③ | C.①③ | D.①④ |
已知C—C单键可以绕键轴旋转,某烃的结构简式如图,下列说法中正确的是()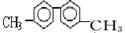
| A.该烃分子中有六种不同环境的氢原子 |
| B.该烃的一氯代物最多有四种 |
| C.分子中至少有10个碳原子处于同一平面上 |
| D.该烃是苯的同系物,能使高锰酸钾和溴水褪色 |
25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数为
| A.12.5% | B.25% | C.50% | D.75% |
“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,如图是异辛烷的球棍模型,则异辛烷的系统命名为()
| A.1,1,3,3-四甲基丁烷 | B.2,3,4-三甲基戊烷 |
| C.2,4,4-三甲基戊烷 | D.2,2,4-三甲基戊烷 |
分析下列有机物的结构判断该有机物可能发生的反应类型()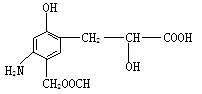
①加成反应 ②消去反应 ③取代反应 ④水解反应 ⑤中和反应 ⑥显色反应 ⑦氧化反应
| A.全部 | B.除④外其余都有 | C.只④⑤⑥⑦ | D.只①③⑤⑥⑦ |