某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢。
(1)A的结构简式为 ;
(2)A中的碳原子是否都处于同一平面? (填“是”或者“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。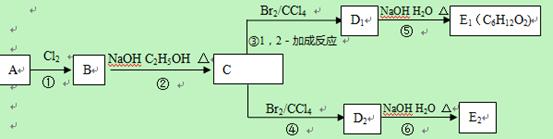
反应②的化学方程式为
;
C的化学名称为 ;
E2的结构简式是 ;
④、⑥的反应类型依次是 
 、 。
、 。
某课外活动小组利用下图装置进行乙醇的催化氧化实验制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白:
(1)甲装置常常浸在70~80℃的水浴中,目的是。
(2)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。
①乙醇的催化氧化反应是________反应(填“放热”或“吸热”),该反应的化学方程式为。
②控制鼓气速度的方法是控制甲中单位时间内的气泡数,若鼓气速度过快,则会,若鼓气速度过慢则会反应放热太少,不能达到反应所需温度。
(3)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接、_______接丙。
(4)简述如何验证丁装置中乙醛的存在。
在呼吸面具和潜水艇中可用过氧化纳作为供氧剂。请选用适当的化学试剂和实验用品、用上图中的实验装置进行实验,证明过氧化钠可作供氧剂。
(1)A是实验室制取CO2的装置。写出A中发生反应的离子方程式:。
(2)B装置中装有饱和的NaHCO3溶液,其作用是: 。
(3)写出过氧化钠与二氧化碳反应的化学方程式:。
该反应中氧化剂是,还原剂是,反应过程中氧化剂与还原剂的物质的量之比为。
某同学欲配制450mL 0.1mol/L的碳酸钠溶液,试根据所学回答下列问题。
(1)若采用5mol/L的碳酸钠溶液配制溶液,需要用到碳酸钠溶液的体积为。
(2)若用碳酸钠固体配制,一定会用到的仪器有________________________
A.450ml容量瓶 B.500 ml容量瓶 C.量筒 D.胶头滴管
E.烧杯 F.玻璃棒 G.托盘天平
(3)欲准确配制所需溶液,下列称量质量正确的是()
A.称Na2CO3 4.8克 B.Na2CO3 5.3克
C.称Na2CO3·10H2O 12.87克 D.称Na2CO3·10H2O 14.30克
(4)若在配溶液的过程中用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是________(填序号)。
A.吸出多余液体,使凹液面与刻度线相切
B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的碳酸钠固体
D.重新配制
(5)下列操作可能导致结果偏高的是。
A.转移后没有洗涤烧杯
B.定容时俯视
C.定容时仰视
D.称取的Na2CO3溶液中混有少量Na2CO3·10H2O
E.配溶液前用碳酸钠溶液润洗容量瓶
(9分)某化学兴趣小组对生石灰与水反应是显著放热反应进行了实验探究,在除了用手触摸试管壁感觉发热外,还设计了下列几个可行性方案。
甲方案:将温度计与盛放有生石灰的小试管用橡皮筋捆绑在一起,放入有水的小烧杯中,用胶头滴管向小试管中缓缓滴入水,看到的现象是,说明反应放热。(下列装置中支撑及捆绑等仪器已略去)
乙方案:将盛放有生石灰的小试管插入带支管的试管中,支管接①或②,用胶头滴管向小试管中缓缓滴入水,看到的现象是(接①),(接②),说明反应放热。
丙方案:用胶头滴管向盛放有生石灰且带支管的试管中滴加水,支管接的导管中盛适量无水硫酸铜粉末,看到的现象是,说明反应放热,其原因是。
(8分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态)):
 时间(min) 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大, 原因是。
原因是。 (2)哪一段时段的反应速率最小,原因是
(2)哪一段时段的反应速率最小,原因是 。
。 (3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)。 (4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
| A.蒸馏水 | B.NaCl溶液 | C.Na2CO3溶液 | D.CuSO4溶液 |
 你认为可行的是(填编号)。
你认为可行的是(填编号)。