用NA表示阿伏加德罗常数的值,下列说法中不正确的是
| A.17g氨气中含有3NA对共用电子对 |
| B.4.48LN2与CO的混合物所含分子数为0.2NA |
| C.16g甲烷与足量的氯气在强光作用下最多可得4NA个HCl分子 |
| D.0.2 mol C2H6O分子中一定存在0.2NA个碳碳单键 |
列有关化学用语表达不正确的是
A.氨气分子的电子式: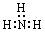 |
| B.CS2分子的结构式: S=C=S |
C.S2-的结构示意图: 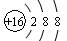 |
D.CH4的分子模型示意图为: |
绿色交通工具是指在行驶中对环境不发生污染或只发生微量污染的载客工具。下列不属于绿色交通工具的是
一定温度下进行反应:COCl2(g) Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
| t/s |
0 |
2 |
4 |
6 |
8 |
| n(Cl2)/mol |
0 |
0.30 |
0.39 |
0.40 |
0.40 |
下列说法不正确的是
A.0~4s容器内的压强逐渐增大
B.生成Cl2的平均反应速率,0~2s比2~4s快
C.8s时向容器中再充入一定量的氦气,反应速率又会加快
D.该条件下,COCl2的最大转化率为40%
下列条件中,锌和硫酸开始反应时放出氢气的速率最大的是
| 选项 |
金属 |
酸溶液的浓度和体积 |
温度/℃ |
| A |
2.4 g锌片 |
3 mol·L-1硫酸50 mL |
40 |
| B |
2.4 g锌粉 |
1 mol·L-1硫酸200 mL |
30 |
| C |
2.4 g锌粉 |
3 mol·L-1硫酸50 mL |
40 |
| D |
5.6 g锌片 |
3 mol·L-1硫酸100 mL |
30 |
干电池原理示意图如下,电池总反应为:Zn+2NH4+=Zn2++2NH3↑+H2↑,下列说法正确的是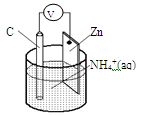
| A.碳为电池的正极 |
| B.Zn极上发生还原反应 |
| C.Zn2+移向该电池的负极 |
| D.反应2NH4++2e-=2NH3↑+H2↑在负极上发生 |