下列关于有机物的说法错误的是:
| A.乙烯和苯都能使溴水褪色,褪色的原因不相同 |
| B.石油和天然气的主要成分都是碳氢化合物 |
| C.苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
| D.甲烷与氯气反应生成一氯甲烷和苯与硝酸反应生成硝基苯的反应类型相同 |
对于反应:4NH3(g) + 5O2(g)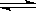 4NO(g) + 6H2O(g), 下列为四种不同情况下测得的反应速率,其中能表明该反应进行最快的是( )
4NO(g) + 6H2O(g), 下列为四种不同情况下测得的反应速率,其中能表明该反应进行最快的是( )
| A.v(NH3)= 0.2mol·L-1·s-1 | B.v(O2 )=" 0.24" mol·L-1·s-1 |
C.v(H2 O )=" 0.25" mol·L-1·s-1 O )=" 0.25" mol·L-1·s-1 |
D.v(NO) =" 0.15" mol·L-1· s-1 s-1 |
反应L(s)+aG(g) bR(g)达到平衡时,温度和压强对该反应的影响如图所示,图中:压强 P1>P2,X轴表示温度,Y轴表示平衡混合气中G的体积分数。
bR(g)达到平衡时,温度和压强对该反应的影响如图所示,图中:压强 P1>P2,X轴表示温度,Y轴表示平衡混合气中G的体积分数。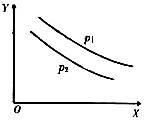
据此可判断( )
| A.上述反应是放热反应 | B.上述反应是吸热反应 |
| C.a>b | D.a=b |
一定条件下反应2AB(g) 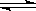 A2(g)+B2(g)达到平衡状态的标志是( )
A2(g)+B2(g)达到平衡状态的标志是( )
A.单位时间内生成nmolA2,同时消耗2n molAB
B.容器内,3种气体AB、A2、B2共存
C.AB的消耗速率等于A2的消耗速率
D.容器中各组分的体积分数不随时间变化
已知充分燃烧a g乙炔(C2H2)气 体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是()
体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是()
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l )ΔH=-2b kJ / mol )ΔH=-2b kJ / mol |
| B.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=b kJ / mol |
| C.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l)ΔH=2b kJ / mol |
| D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-4b kJ / mol |
在密闭容器中,对于反应:2SO2(g)+O2(g)  2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为( )
2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为( )
| A.10 mol和10% | B.20 mol和20% |
| C.20 mol和40% | D.20 mol和80% |