下列各化合物中,能发生酯化、还原、加成、消去四种反应的是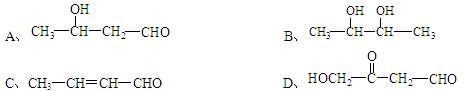
关于Na2CO3、NaHCO3性质的有关叙述不正确的是
| A.热稳定性:Na2CO3>NaHCO3 |
| B.NaHCO3能与NaOH溶液反应而Na2CO3则不能 |
| C.Na2CO3能转化成NaHCO3,而NaHCO3也能转化为Na2CO3 |
| D.等质量的Na2CO3、NaHCO3分别与足量的稀盐酸反应,产生CO2气体的质量相等 |
将7.2gCO和H2的混合气体与足量O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加()
| A.2.1g | B.3.6g | C.7.2g | D.无法确定 |
在水溶液中能大量共存,且加入过量稀硫酸溶液时,有气体生成的是( )
| A.Na+Ag+ CO32-Cl- | B.K+Ba2+ SO42- Cl- |
| C.Na+ K+ CO32- Cl- | D.Na+ K+ Cl-SO42— |
下列离子反应方程式,书写正确的是()
| A.向盐酸中加碳酸钠溶液 CO32- + 2H+ = H2O +CO2↑ |
| B.向稀硫酸溶液中投入铁粉 2Fe +6H+ = 2Fe3+ +3H2↑ |
| C.向盐酸中投入碳酸钙 CO32- + 2H+ = H2O +CO2↑ |
| D.氢氧化钡溶液中加入硫酸 H+ + OH- =H2O |
向澄清石灰水中不断通入二氧化碳气体的过程中,该溶液的导电性的变化是(纵坐标表示导电性,横坐标表示二氧化碳气体的物质的量)