H、C、N、O是几种重要的非金属元素。回答以下问题:
(1)C、N、O三种元素第一电离能从大到小的顺序是 。
(2)H3O+中H—O—H的键角比H2O中H—O—H的键角大,是因为 。
(3)与CO2是等电子体,可检验溶液中Fe3+的阴离子的电子式 。
(4)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮化物。
①肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)==3N2(g)+4H2O(g) △H=-1038.7 kJ/mol
若该反应中有4mol N—H键断裂,则形成的π键有___________mol。
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在________(填标号)
a、离子键 b、共价键 c、配位键 d、范德华力
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是 (填标号)。
a、CF4 b、 CH4 c、 NH4+ d、H2O
实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物是棕红色、易潮解,100℃左右时升华。下图是两个学生设计的实验装置、左边的反应装置相同,而右边的产品收集装置则不同,分别如(Ⅰ)和(Ⅱ)所示。
试回答:
⑴B中反应的离子方程式为:_________________________________________;向B中加入A中的反应液的操作是。
⑵D中的反应开始前,需排除装置中的空气,应采取的方法是:_________________。
⑶D中反应化学方程式为:________________________________,D中的反应现象:
。
⑷装置(Ⅰ)的主要缺点是:____________________________________________。
⑸装置(Ⅱ)的主要缺点是:_____________________________。如果选用此装置来完成实验,则必须采取的改进措施是:____________________________________。
将0.1 mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液至过量。请回答:
(1)写出与铝有关的离子方程式:
(2)若在滴加NaOH溶液过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160mL时,则金属粉末中n(Mg)=mol,
V2=mL。沉淀的最大质量是g。
(3)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=mL。
(4)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:。
某反应体系中的物质有:H2O、NO、HNO3(稀)、NaNO3、Na2S、S。
⑴请将Na2S之外的反应物与生成物分别填入以下框内,使方程式完整!
Na2S +
⑵反应中,被还原的元素是,还原剂是。
⑶将氧化剂与还原剂填入下列空格中,并标出电子转移的方向和数目。
+…
⑷实验室制备H2S 气体应选用的酸,如(举一例)
⑸纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,不用写方程式判断还原剂与氧化剂物质的量之比为。
对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系.下表是25℃时几种常见弱酸的电离平衡常数
| 酸 |
电离方程式 |
电离平衡常数K |
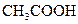 |
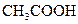   |
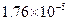 |
 |
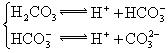 |
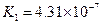 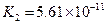 |
 |
 |
 |
 |
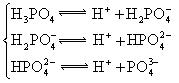 |
   |
回答下列各问:
(1)K只与温度有关,当温度升高时,K值________(填“增大”、“减小”、“不变”).
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?__________________.
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是_________,最弱的是________.
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数.对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,对于H3PO4此规律是________________,产生此规律的原因是_________________________.
(5)电离平衡常数是用实验的方法测定出来的.现已经测得某温度下 NH3∙H2O溶液中存在如下反应:NH3∙H2O NH4++OH-已知0.10 mol·L-1 NH3∙H2O溶液中,达到平衡时,C平衡(OH-)="4.2" × 10-3mol·L-1,C平衡(NH3∙H2O)≈C起始(NH3∙H2O),水的电离可忽略不计;
①用pH试纸测量溶液的pH值,即可求得C平衡(OH-),测定溶液pH值的操作是______________。
②测量C平衡(NH3∙H2O)的方法最好用_____________法(填方法名称)
③求此温度下该反应的平衡常数K.(写出计算过程,计算结果保留2位有效数字)
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,生成4mol z时放出热量Q KJ, 它们的物质的量随时间的变化如表所示。
| t/min |
X/mol |
Y/mol |
Z/mol |
| 0 |
1.00 |
1.00 |
0.00 |
| 1 |
0.90 |
0.80 |
0.20 |
| 3 |
0.75 |
0.50 |
0.50 |
| 5 |
0.65 |
0.30 |
0.70 |
| 9 |
0.55 |
0.10 |
0.90 |
| 10 |
0.55 |
0.10 |
0.90 |
| 14 |
0.55 |
0.10 |
0.90 |
(1)根据上表中数据,在答卷该题相应位置上画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
(2) 写出体系中发生反应的热化学方程式 ______;
(3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:
(4) 该反应达到平衡时反应物X的转化率 等于______________________;
等于______________________;
(5) 改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是:1 _____2_____3_____的曲线: