在一个固定体积的密闭容器中,加入2molA和1molB发生以下反应:2A(g)+B(g)  3C(g)+D(g),达到平衡时C的浓度为W moll/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡时,D的浓度为W/3 moll/L的是
3C(g)+D(g),达到平衡时C的浓度为W moll/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡时,D的浓度为W/3 moll/L的是
| A.3molC+1molD |
| B.2molA+2mol C |
| C.2molA+1moB+0.5molD |
| D.1molA+0.5molB+1.5molC+0.5molD |
下列有机物名称正确的是
| A.2-乙基戊烷 | B.1,2-二氯丁烷 |
| C.2,2-二甲基-4-己醇 | D.3,4-二甲基戊烷 |
有机物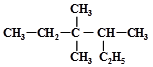 的正确命名为
的正确命名为
| A.2-乙基-3,3-二甲基-4-乙基戊烷 | B.3,3-二甲基-4-乙基戊烷 |
| C.3,3,4-三甲基己烷 | D.2,3,3-三甲基己烷 |
下列化合物的核磁共振氢谱中出现三个峰的是
| A.2,2,3,3四甲基丁烷 | B.2,3,4三甲基戊烷 |
| C.3,4二甲基己烷 | D.2,5二甲基己烷 |
下列表示的是正丙基的是
| A.CH3CH2CH3 | B.CH3 CH2CH2- |
| C.―CH2CH2CH2― | D.(CH3 )2CH- |
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
| A.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+ |
| B.外电路中电子由c电极流向VB2电极 |
| C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生 |
| D.若B装置内的液体体积为200 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |