市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应为: Li+2Li
Li+2Li
 下列说法不正确的是
下列说法不正确的是
A.放电时,负极的电极反应式:Li-e-=Li+ |
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应 |
C.该电池不能用水溶液作为电解质 |
D.放电过程中Li+向负极移动 |
下表中实验操作、现象和所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
用激光笔照射鸡蛋白水溶液 |
有丁达尔效应 |
鸡蛋白分子直径介于1nm~100nm |
| B |
向某氯化亚铁溶液中加入Na2O2粉末 |
出现红褐色沉淀 |
说明原氯化亚铁已氧化变质 |
| C |
碳酸盐X加热分解,产生的气体通入酸化的BaCl2溶液 |
产生白色沉淀 |
X可能是NaHCO3 |
| D |
湿润的KI淀粉试纸靠近气体Y |
试纸变蓝 |
Y一定是Cl2 |
下列离子方程式与所述事实相符且正确的是
| A.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| B.向含有0.4molFeBr2的溶液中通入0.3molCl2充分反应: 4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
| C.向明矾溶液中加入Ba(OH)2溶液至生成的沉淀物质的量最多: Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D.磁性氧化铁溶于稀硝酸:Fe3O4+8H++NO3-=3Fe3++NO↑+4H2O |
下列各组离子在相应的条件下一定能大量共存的是
| A.在碱性溶液中:CO32-、K+、S2-、Na+ |
| B.与铝粉反应放出氢气的无色溶液中:NO3-、Mg2+、Na+、SO42- |
| C.在c(H+)/c(OH-)=1×1012的溶液中:NH4+、AlO2-、C1-、K+ |
| D.在中性溶液中:Fe3+、C1-、NO3-、A13+ |
下列离子或分子组在溶液中能大量共存,且满足相应要求的是
| 选项 |
离子 |
要求 |
| A |
K+、NO3-、Cl-、HS- |
c(K+)<c(Cl-) |
| B |
Fe3+、NO3-、S2-、Cl- |
逐滴滴加盐酸立即有气体产生 |
| C |
Na+、HCO3-、Mg2+、SO42- |
逐滴滴加氨水立即有沉淀产生 |
| D |
NO3-、Al3+、NH4+、CH3COOH |
滴加NaOH浓溶液立即有气体产生 |
下列实验中,所选装置或实验设计合理的是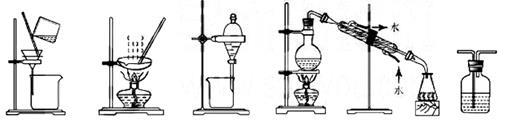
① ② ③ ④ ⑤
| A.图⑤所示装置中盛有饱和Na2SO3溶液除去SO2中含有的少量HCl |
| B.用乙醇提取碘水中的碘选择图③所示装置 |
| C.用图①和②所示装置进行粗盐提纯 |
| D.用图④所示装置进行石油分馏实验制取汽油 |