下列说法正确的是
| A.将Ca(OH)2饱和溶液加热,溶液的pH增大 |
| B.常温下,pH=11的氨水与pH=3的盐酸等体积混合后,溶液的pH>7 |
| C.将0.1mol/L的HI溶液加水稀释l00倍,溶液中所有离子的浓度随之减小 |
| D.两种醋酸溶液的pH分别为a和(a+1),物质的量浓度分别为c1和c2,则有c1=10c2 |
某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:
①5 mL水
②20 mL 0.5 mol·L-1的Na2SO4溶液
③40 mL 0.2 mol·L-1的Ba(OH)2溶液
④40 mL 0.1 mol·L-1的H2SO4溶液中,溶解至饱和
以上各溶液中,c(Ba2+)的大小顺序正确的是( )
| A.③>①>④>② | B.③>①>②>④ |
| C.①>④>③>② | D.①>③>④>② |
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目减少 |
B.溶液中 不变 不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10 mL pH=11的NaOH溶液,混合液pH=7 |
下列叙述正确的是( )
| A.中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多于醋酸 |
| B.将氢氧化钠溶液和氨水各稀释一倍,两者的c(OH-)均减少到原来的一半 |
| C.常温下,某溶液中由水电离出的c(OH-)=1×10-10 mol/L,该溶液可能是盐酸 |
| D.如果盐酸的物质的量浓度是醋酸的两倍,则盐酸的c(H+)也是醋酸的两倍 |
莫尔盐[(NH4)2Fe(SO4)2·6H2O]常作氧化还原滴定法的基准物质,下列有关该盐溶液的比较,不正确的是( )
A.c(SO )>c(NH )>c(NH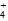 )>c(Fe2+)>c(H+)>c(OH-) )>c(Fe2+)>c(H+)>c(OH-) |
B.c(SO )=c(NH )=c(NH )>c(Fe2+)>c(H+)>c(OH-) )>c(Fe2+)>c(H+)>c(OH-) |
C.2c(SO )+c(OH-)=c(NH )+c(OH-)=c(NH )+2c(Fe2+)+c(H+) )+2c(Fe2+)+c(H+) |
D.c(NH )+c(NH3·H2O)=2c(Fe2+)+2c[Fe(OH)2] )+c(NH3·H2O)=2c(Fe2+)+2c[Fe(OH)2] |
下列说法正确的是( )
| A.25℃时 NH4Cl 溶液的 KW大于 100℃时 NaCl 溶液的 KW |
B.SO2通入碘水中,反应的离子方程式为 SO2+I2+2H2O=SO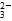 +2I-+4H+ +2I-+4H+ |
C.加入铝粉能产生 H2的溶液中,可能存在大量的 Na+、Ba2+、AlO 、NO 、NO |
| D.100℃时,将 pH =2 的盐酸与 pH =12 的 NaOH 溶液等体积混合,溶液显中性 |