某全钒新型电池,以惰性材料作电极,在电解质溶液中发生电池总反应为:
下列说法正确的是
| A.当电池无法放电时,只要更换电解质溶液,不用外接电源进行充电就可正常工作 |
B.放电时,负极反应为 |
| C.充电时,阳极附近溶液由绿色逐渐变为紫色 |
| D.放电过程中,正极附近溶液的pH变小 |
有按如下特点排列的一系列(n种)稠环芳香烃:
①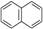 ②
② ③
③ ④
④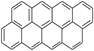
该系列化合物中所含碳的质量分数最大值是()
| A.93.8% | B.95.7% | C.97.3% | D.无法确定 |
已知分子式为C12H12的物质a的结构简式为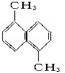 ,其苯环上的二溴代物有9种同分异构体,由此推断a苯环上的四溴代物的同分异构体的数目有()
,其苯环上的二溴代物有9种同分异构体,由此推断a苯环上的四溴代物的同分异构体的数目有()
| A.9种 | B.10种 | C.11种 | D.12种 |
两种气态烷烃的混合物,在标准状况下其密度为1.16 g/L,则关于此混合物组成的说法正确的是( )
| A.一定有甲烷 |
| B.一定有乙烷 |
| C.可能是甲烷和戊烷的混合物 |
| D.可能是乙烷和丙烷的混合物 |
有机物CH3—CH==CH—CI能发生的反应有()
①取代反应
②加成反应
③消去反应
④使溴水褪色
⑤使酸性KMnO4溶液褪色
⑥与AgNO3溶液生成白色沉淀
⑦聚合反应
| A.以上反应均可发生 |
| B.只有⑦不能发生 |
| C.只有⑥不能发生 |
| D.只有②不能发生 |
下列不属于消去反应的是()