高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是
| A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质 |
| B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质 |
| C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌 |
| D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌 |
常温下,将pH=1的硫酸溶液平均分成两等份,一份加入适量水,另一份加入与该硫酸溶液物质的量浓度相同的氢氧化钠溶液,两者pH都升高了1,则加入的水和氢氧化钠溶液的体积比为( )
| A.5:1 | B.6:1 | C.10:1 | D.11:1 |
在蒸发皿中用酒精灯加热蒸干下列物质的溶液然后灼烧,可得到该物质固体的是()
| A.Al2(SO4)3 | B.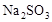 |
C.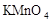 |
D.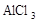 |
T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论正确的是()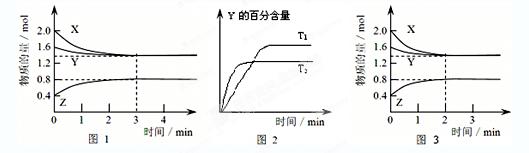
| A.反应进行的前3 min内,用X表示的反应速率 v(X)=0.3mol/(L·min) |
B.容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
现有强酸甲溶液的pH=1,强酸乙溶液的pH=2,则酸甲与酸乙的物质的量浓度之比不可能的是( )
| A.2∶1 | B.5∶1 | C.10∶1 | D.20∶1 |
某化学反应其△H=" —122" kJ·mol-1,∆S=" —231" J·mol-1·K-1,则此反应在下列哪种情况下可自发进行( )
| A.在任何温度下都能自发进行 | B.在任何温度下都不能自发进行 |
| C.仅在高温下自发进行 | D.仅在低温下自发进行 |