下列烷烃在光照下与氯气反应,生成的一氯代烃只有一种的是
下列变化过程中,共价键被破坏的是
| A.烧碱固体溶于水 | B.氯化氢气体溶于水 |
| C.二氧化碳变成干冰 | D.碘溶于酒精 |
有A、B和C三种主族元素,若A元素阴离子与B、C元素的阳离子具有相同的电子层结构,且B的阳离子半径大于C,则这三种元素的原子序数大小次序是
A.B<C<A B.A<B<C C.C<B<A D.B>C>A
下列各组元素按电负性大小排列正确的是
| A.F>N>O | B.O>Cl>F | C.As>P>H | D.Cl>S>As |
下列金属冶炼的反应原理,错误的是
A.2NaCl(熔融) 2Na + Cl2↑ 2Na + Cl2↑ |
B.MgO + H2 Mg + H2O Mg + H2O |
C.Fe3O4 + 4CO 3Fe + 4CO2 3Fe + 4CO2 |
D.2HgO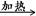 2Hg + O2↑ 2Hg + O2↑ |
下列性质中,可以证明某化合物中一定存在离子键的是
| A.可溶于水 | B.具有较高的熔点 |
| C.水溶液能导电 | D.熔融状态能导电 |