能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上合成甲醇的反应原理为:CO(g) + 2H2(g)  CH3OH(g) ΔH,下表所列数据是该反应在不同温度下的化学平衡常数(K)。
CH3OH(g) ΔH,下表所列数据是该反应在不同温度下的化学平衡常数(K)。
①根据表中数据可判断ΔH 0 (填“>”、“=”或“<”)。
②在300℃时,将2 mol CO、3 mol H2和2 mol CH3OH充入容积为1L的密闭容器中,此时反应将 。
| A.向正方向移动 | B.向逆方向移动 | C.处于平衡状态 | D.无法判断 |
(2)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH=-1451.6 kJ·mol-1
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ·mol-1
写出该条件下甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(3)以甲醇、氧气为原料,KOH溶液作为电解质构成燃料电池总反应为:2CH3OH+3O2+4OH-=2CO32-+6H2O,则负极的电极反应式为 ,随着反应的不断进行溶液的pH (填“增大”“减小”或“不变”)。
(4)如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为 ;如果电解一段时间后NaCl溶液的体积为1L,溶液的pH为12(25℃下测定),则理论上消耗氧气的体积为 mL(标况下)。
已知A、E是生活中常见的两种有机物;B是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平;A能在酸性高锰酸钾的条件下生成E; C是高分子化合物。在一定条件下由A可以转变为有机物B、C、D、E、F(A、B、D、E碳原子数相等)。转变关系如下: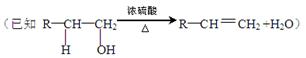
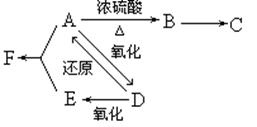
请回答下列问题:
(1)B的电子式是____________。
(2) E的官能团名称是____________。
(3) 写出实现下列转化的化学方程式
①A→D
② B→C
(4) A是一种高效、低耗、污染小的可再生的清洁能源,已知1molA完全燃烧生成CO2气体和水蒸气放出1367kJ热量,则在相同条件下,1molA完全燃烧生成CO2气体和液态水,放出的热量________1367kJ(填“>”、“=”或“<”)。
(5) 在可逆反应当中,产率指的是某种生成物的实际产量与理论产量的比值.若100克A和120克E反应生成了88克F,则F的产率是____________(用百分数表示)
(6)下列关于A、B、C、D、E、F六种物质说法正确的是____________
A.C具有固定的元素组成,因而有固定的熔沸点
B.C中有不饱和键,所以能使高锰酸钾溶液褪色
C. 取等物质的量的B和C完全燃烧后,生成的CO2和H2O的物质的量分别相等
D.由B生成C是通过加聚反应制得的
E. 分别燃烧1molA和B生成CO2和H2O的耗氧气量,其中A和B耗氧量相等
F.在 A+E→ F转变中,有含氧的小分子生成,小分子的氧原子来至于A
如图在试管Ⅰ中先加入3mL 95%的乙醇, 并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2mL无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管Ⅱ中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管Ⅰ小火加热3~5min后,改用大火加热,当观察到试管Ⅰ中有明显现象时停止加热。试回答:
试管Ⅱ中的导管不插入液面下的原因是;
(2)反应完毕后,振荡试管Ⅱ,观察到试管Ⅱ中的现象是;
(3)试管Ⅰ中加入浓硫酸的作用是 ;
(4)本实验反应开始时用小火加热的原因是 ________;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(5)试管Ⅱ中饱和Na2CO3的作用是
(6)写出试管Ⅰ中发生反应的化学方程式
该反应的反应类型是
有①甲烷,②乙烷,③丙烷,④丁烷4种烷烃,试回答下列问题:
(1)请写出烷烃(用通式表示)在足量的氧气中充分燃烧的化学方程式:
________________________________________________________________________。
(2)相同状况下,等体积的上述气态烃,消耗O2的量最多的是________。
(3)等质量的上述气态烃,在充分燃烧时,消耗O2的量最多的是________。
(4)存在同分异构体的是________。
(5)在120 ℃,1.01×105Pa条件下,某气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃为________。
(6)10 mL某气态烃,在50 mL O2中充分燃烧,得到液态水,以及体积为35 mL的混合气体(所有气体体积均在同温同压下测定)。该气态烃是________。
(1)如下图所示,组成一种原电池.试回答下列问题(灯泡功率合适):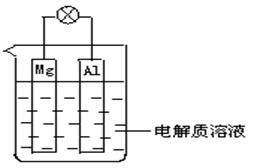
①电解质溶液为稀H2SO4时上述装置中灯泡亮,此时Al电极上发生反应的电极反应式为: ___;
②电解质溶液为NaOH溶液时,灯泡__________(填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Al电极上发生反应的电极反应式为:_______________;
b.若灯泡不亮,其理由为:________________________。
(2)原电池原理的应用之一是可以设计原电池。请利用反应“Cu+2Fe3+ =2Fe2+ +Cu2+ ”设制一个原电池(正极材料用碳棒)则该电池的负极材料是,正极上发生反应的电极反应式;若导线上转移电子1.5 mol,则溶解铜的质量是。另外的重要应用是实验室在用锌与稀硫酸反应制备氢气时,可向溶液中滴加少量硫酸铜溶液,其作用是:。
将锌片和铜片以下图所示两种方式分别插入同浓度稀硫酸中。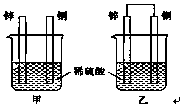
(1)以下叙述中,正确的是(填标号)。
| A.装置甲、乙中铜片表面均无气泡产生 |
| B.装置甲、乙中稀硫酸的浓度均减小 |
| C.装置乙中锌片是正极,铜片是负极 |
| D.装置乙中产生气泡的速率比装置甲快 |
(2)装置乙中,总反应的离子方程式为 ;若导线上通过0.2 mol电子,消耗锌的质量为 g。