(5分) 请观察下图装置,回答下列问题: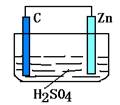
(1) 负极是________,发生_______反应(填氧化或还原)
(2) 正极是________,发生_______反应(填氧化或还原)
(3) 正极的电极反应式:__________________________.
实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。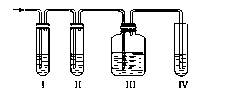
(1)写出实验室制乙烯的反应方程式:
(2)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:Ⅰ___________;Ⅱ___________;Ⅲ___________;Ⅳ:浓溴水(将下列有关试剂的序号填入空格内)。
| A.品红溶液 | B.NaOH溶液 | C.浓H2SO4 | D.酸性KMnO4溶液 |
(3)能说明二氧化硫气体存在的现象是_______________________________。
(4)确证含有乙烯的现象是_________________________________________。
(5)写出Ⅳ中发生反应的化学方程式:。
写出下列有机物的结构简式:
(1)2,6-二甲基-4-乙基辛烷:;
(2)2-甲基-1-戊烯:;
(3)有A、B、C三种烃,它们的结构简式如下图所示: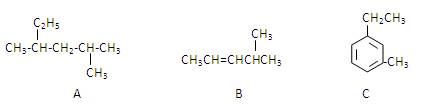
A的名称是;B的名称是;
C的名称是。
选择下列某种答案的序号, 填入下表的空格
①同位素②同素异形体③同分异构体④同系物⑤同种物质
| 物质 |
丁烷与 |
红磷 |
氯仿与 |
氕与 |
新戊烷与 |
| 名称 |
2--甲基丙烷 |
与白磷 |
三氯甲烷 |
氘、氚 |
2,2--二甲基丁烷 |
| 相互 |
|||||
| 关系 |
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第I B族。Cu2+的核外电子排布式为 ▲。
(2)右图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 ▲。
(3)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如下: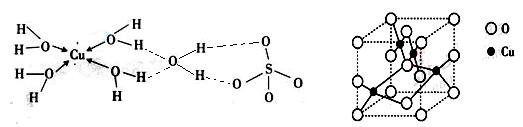
下列说法正确的是 ▲(填字母)。
| A.在上述结构示意图中,所有氧原子都采用sp3杂化 |
| B.在上述结构示意图中,存在配位键、共价键和离子键 |
| C.胆矾是分子晶体,分子间存在氢键 |
| D.胆矾中的水在不同温度下会分步失去 |
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 ▲。
酞菁也是常见的配位体,结构如右图。该分子中氮原子杂化方式为 ▲。 写出与硫酸根离子互为等电子体的分子和离子各一种 ▲、 ▲。
(5)Cu2O的熔点比Cu2S的 ▲(填“高”或“低”),
请解释原因 ▲。
硫酸钙是一种用途非常广泛的产品。
(1)25℃时,Ksp(CaSO4)=7.10×10-5。在1L0.1mol·L-1CaCl2溶液中加入1L0.2mol·L-1的Na2SO4溶液,充分反应后(假设混合后溶液的体积变化忽略不计)溶液中Ca2+物质的量的浓度为 ▲mol·L-1。
(2)某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体放在坩埚中加热,经测量剩余固体质量随时间变化如图所示。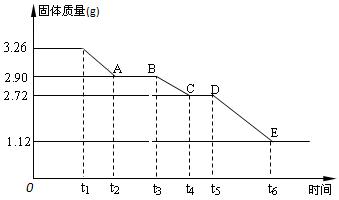
①x :y =____▲_____。
②② t2~t3时间段固体的化学式为 ▲。
③ t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色,则该时间段所发生反应的化学方程式为。