化学反应N2+3H2= 2NH3的能量变化如下图所示,该反应的热化学方程式是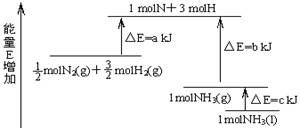
| A.N2(g)+3H2(g)=2NH3 (l)△H=2(a—b—c)kJ·mol-1 |
| B.N2(g)+3H2(g)=2NH3(g) △H=2(b—a)kJ·mol-1 |
| C.1/2N2(g)+3/2H2(g)=NH3(l) △H=(b+c—a)kJ·mol-1: |
| D.1/2N2(g)+3/2H2(g)=NH3(g) △H=(a+b)kJ·mol-1 |
由CO2、H2和CO组成的混合气在同温同压下与氮气的密度相同.则该混合气体中CO2、H2和CO的体积比可能为()
| A.29∶8∶13 | B.22∶1∶14 | C.13∶8∶29 | D.29∶16∶57 |
相同体积的氯化钠、氯化镁、氯化铝溶液分别与过量的硝酸银溶液反应,所生成的沉淀物质的量相同,则原氯化钠、氯化镁、氯化铝溶液的物质的量浓度之比为( )
| A.1 :2 :3 | B.3 :2 :1 | C.6 :3 :1 | D.6 :3 :2 |
已知溶质质量分数为96%的酒精溶液的物质的量浓度为16.6 mol/L,试判断48%的酒精溶液的物质的量浓度(mol/L)(已知酒精的密度小于1) ()
| A.大于8.3 | B.等于8.3 | C.小于8.3 | D.无法确定 |
下列对0.3mo1/LNa2SO4溶液叙述不正确的是()
| A.1L溶液中含0.3NA个Na+ |
| B.1L溶液中含Na+和SO42-总数为0.9NA |
| C.2L溶液中含有0.6NA个SO42- |
| D.2L溶液中Na+的物质的量浓度为0.6mol/L |
在同温同压下,A容器的H2和B容器的NH3,若所含原子总数相等,则这两个容器的体积比是( )
| A.2∶ 1 | B.1∶ 2 | C.2∶ 3 | D.1∶ 3 |