下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题: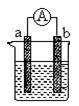
(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
。
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置 (填“能”或“不能”)形成原电池,若不能,请说明理由,若能,请指出正、负极 。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。
现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用碱性溶液为电解液;则氢气应通入 极(填a或b,下同),电子从 极流出。a极发生电极反应式为:_____________________________。
(共8分) A、B、C、D、E是短周期元素,周期表中A与B、B与C相邻;A与E的最外层电子数之比为2:3,B的最外层电子数比E的最外层电子数少1个;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红。
(1) E的元素符号是__________。
(2)A、B、C的氢化物稳定性由强到弱的顺序为(用分子式表示)__________________;B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z的晶体类型为____________;用电子式表示AE2的形成过程________________________。
(3)由A、B、C、D、E中的一种或几种元素组成的物质来检验Fe3+的离子方程式为__________________________。
(共10分) W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素。Y和W的最外层电子数相等。Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。由此可知:
(1)写出元素名称:W_________,X________,Y________,Z_________;Z在元素周期表中的位置_________。
(2)Y2Z的电子式为_________;W2X2的结构式__________。
(3)两种均含四种元素的化合物相互反应放出气体的化学方程式是_______
(共6分)(1)已知CH4(g)+2O2 (g) = CO2 (g) +2H2O (l); △H=-890kJ/mol,现有CH4和CO共0.75mol,完全燃烧后生成CO2气体和18g液态水,并放出515kJ热量,则CO燃烧的热化学方程式为;
(2)化学反应N2+3H2 2NH3的能量变化如图所示,写出生成氨气时该反应的热化学方程式。
2NH3的能量变化如图所示,写出生成氨气时该反应的热化学方程式。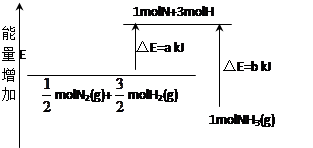
(共6分)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学反应方程式为 ;
(2)反应开始至2minZ的平均反应速率为 ;
(3)若不改变外界条件,5min ~ 6min Z的生成速率(V1)与6min后Z的生成速率(V2)的大小关系为:V1 V2(填大于、小于或等于)。
(11分)A、B、C、D、E五种物质转化关系如图所示: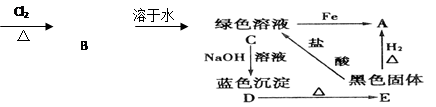
A(单质)棕黄色的烟
(1)确定A、B、C、D、E各为什么物质:(写出各物质的化学式)
A,B,C,D,E。
(2)写出下列各步反应的化学方程式:
E→A:
C→D:
E→C:
A→B: