下列实验操作或装置正确的是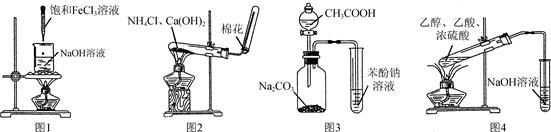
| A.利用图1所示操作制备氢氧化铁胶体 |
| B.利用图2所示装置制取NH3 |
| C.利用图3所示装置证明H2CO3酸性强于苯酚 |
| D.利用图4所示装置制备乙酸乙酯 |
下列有关物质的性质与应用的叙述都正确的是
| A.明矾溶液具有强氧化性,可用作净水剂 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
| D.常温下,铝能被浓硝酸钝化,可用铝制槽车运送浓硝酸 |
25 ℃时,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1 mol·L-1NH4HCO3溶液:K+、Na+、SO42-、OH- |
| B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| C.0.1 mol·L-1CH3COONa溶液:Mg2+、H+、Cl-、SO42- |
| D.Kw/c(H+)=0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3- |
下列有关化学用语表示正确的是
A.中子数为20的氯原子: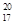 Cl Cl |
| B.苯的结构简式:C6H6 |
C.硅的原子结构示意图: |
D.Na2S的电子式: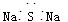 |
国务院办公厅2014年5月印发了《2014~2015年节能减排低碳发展行动方案》。下列做法违背低碳发展原则的是
| A.发展氢能和太阳能 |
| B.限制塑料制品的使用 |
| C.提高原子利用率,发展绿色化学 |
| D.尽量用纯液态有机物代替水作溶剂 |