一个价电子构型为2s22p5的元素,下列有关它的描述正确的有
| A.原子序数为7 | B.周期表中第一电离能最小 |
| C.周期表中电负性最大 | D.周期表中原子半径最大 |
下列关于物质应用和组成的说法正确的是
| A.P2O5可用于干燥Cl2和NH3 |
| B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
| C.CCl4不可用于鉴别溴水和碘水 |
| D.Si和SiO2都用于制造光导纤维 |
某实验小组利用粗硅与氯气反应生成SiCl4粗产品(含有FeCl3、AlCl3等杂质且SiCl4遇水极易水解),蒸馏得四氯化硅(SiCl4的沸点57.7℃),再用氢气还原制得高纯硅;用滴定法测定蒸馏后残留物(将残留物预处理成Fe2+)中铁元素含量。采取的主要操作如图,能达到实验目的是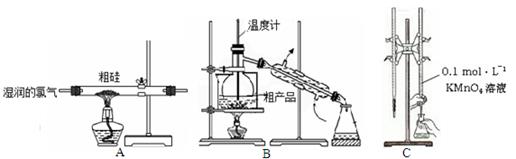
| A.用装置A完成SiCl4的制备 |
| B.用装置B进行蒸馏提纯SiCl4 |
| C.用装置C进行滴定达终点时现象是:锥形瓶内溶液变为紫红色且半分钟内不变色 |
| D.配制0.1 mol·L—1 KMnO4溶液定容摇匀后,发现液面低于刻度线,加水至刻度线 |
向Ba(OH)2和NaOH混合溶液中缓缓通入CO2气体至过量,生成沉淀物质的量与通入CO2气体的体积V(标准状况)的关系如图所示,下列结论不正确的是
A.原混合物中n[Ba(OH)2]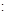 n[NaOH]=1:2 n[NaOH]=1:2 |
| B.横坐标轴上p点的值为90 |
| C.b点时溶质为NaHCO3 |
D.ab段发生反应的离子方程式依次为:CO2+2OH- = H2O+CO32-,CO2 H2O+ CO32- = 2HCO3- H2O+ CO32- = 2HCO3- |
现有KCl和KBr的混合物3.87 g,将混合物全部溶于水,并加入过量的AgNO3溶液,充分反应后产生6.63 g沉淀物,则原混合物中钾元素的质量分数为
| A.24.1% | B.25.9% | C.40.3% | D.48.1% |
将11.2g的Mg—Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体。再向所得溶液中加入适量的NaOH溶液,产生21.4g沉淀。根据题意推断气体x的成分可能是
| A.0.3mol NO2和0.3mol NO |
| B.0.2mol NO2和0.1mol N2O4 |
| C.0.1mol NO、0.2mol NO2和0.05mol N2O4 |
| D.0.6mol NO |