几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
W |
V |
| 原子半径/nm |
0.090 |
0.118 |
0.075 |
0.073 |
0.102 |
| 主要化合价 |
+2 |
+3 |
+5、+3、-3 |
-2 |
+6、-2 |
下列叙述不正确的是
A.X、Z、W位于同周期,Y与V位于同周期
B.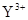 与
与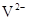 的核外电子数相等
的核外电子数相等
C.Y与W形成的化合物具有两性
D.Z的氢化物可与V的最高价氧化物的水溶液反应生成盐
一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合下图的是( )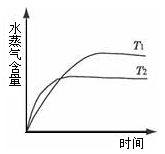
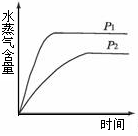
温度(T)的影响 压强(p)的影响
A.CO2(g)+2NH3(g) 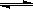 CO(NH2)2(s) + H2O(g);△H<0 CO(NH2)2(s) + H2O(g);△H<0 |
B.CO2(g)+ H2(g) 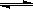 CO(g) + H2O(g);△H>0 CO(g) + H2O(g);△H>0 |
C.CH3CH2OH(g) 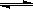 CH2=CH2(g) + H2O(g);△H>0 CH2=CH2(g) + H2O(g);△H>0 |
D.2C6H5CH2CH3(g) + O2(g )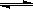 2C6H5CH=CH2(g) + 2 H2O(g);△H<0 2C6H5CH=CH2(g) + 2 H2O(g);△H<0 |
下列实验方案中不能实现:Fe+H2SO4=FeSO4+H2↑反应的是
| A.用导线将铁片和铜片连接后,放入一盛有稀 H2SO4溶液的烧杯中 |
| B.Cu片作阳极,铁片作阴极,电解一定量的H2SO4溶液 |
| C.Cu片作阴极,铁片作阳极,电解一定量的H2SO4溶液 |
| D.将铁片直接放入一盛有稀 H2SO4溶液的烧杯中 |
被称之为“软电池”的纸质电池,其电池总反应Zn+2MnO2+H2O ZnO+2MnO(OH)。下列说法正确的是 ( )
ZnO+2MnO(OH)。下列说法正确的是 ( )
| A.该电池的正极为锌 |
| B.该电池反应中二氧化锰起催化剂作用 |
| C.当65g Zn完全溶解时,流经电极的电子1mol |
D.电池正极反应式为MnO2+e-+H2O MnO(OH)+OH- MnO(OH)+OH- |
能影响水的电离平衡,并使溶液中c(H+)>c(OH-)的操作是()
| A.向水中投入一小块金属钠 | B.将水加热煮沸 |
| C.向水中通入CO2 | D.向水中加入食盐晶体 |
将1 mL 0.1 mol·L-1的H2SO4溶液加入纯水中制成200 mL溶液,该溶液中由水自身电离产生的c(H+)最接近于()
| A.1×10-3 mol·L-1 | B.1×10-11 mol·L-1 |
| C.1×10-7 mol·L-1 | D.1×10-13 mol·L-1 |