下列反应中生成H2的速率最快的是
| |
金属 |
酸溶液 |
温度 |
| A |
Mg |
0.5mol•L-1H2SO4 |
20℃ |
| B |
Fe |
1 mol•L-1HCl |
20℃ |
| C |
Zn |
2 mol•L-1HCl |
20℃ |
| D |
Mg |
1 mol•L-1H2SO4 |
30℃ |
在下列反应中, HCl 作氧化剂的是()
A.NaOH+HCl=NaCl+H2O |
B.Zn+2HCl=ZnCl2+H2↑ |
C.MnO2+4HCl(浓)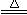 MnCl2+2H2O+Cl2↑ MnCl2+2H2O+Cl2↑ |
D.CuO+2HCl=CuCl2+H2O |
查阅资料发现,金属钠不仅能跟氧气和水反应,还能跟多种其他物质发生反应,其中包括与酒精在常温下反应。要研究金属钠跟酒精反应的性质以及它与金属钠跟水反应的异同点,下列研究方法中用不着的是()
| A.实验法 | B.观察法 | C.分类法 | D.比较法 |
NO和CO都是汽车尾气里的有害物质,有人提出通过以下反应来处理尾 气:
气:
2NO(g ) + 2CO(g ) =N2 (g ) + 2CO2 (g )。 对上述反应,下列看法正确的是()
| A.使用催化剂能加快反应速率 |
| B.改变压强对反应速率没有影响 |
| C.冬天气温低,反应速率降低,对人体危害较小 |
| D.无论外界条件怎样改变,均对此化学反应的速率无影响 |
有X、Y、Z、M四种金属,已知:X可以从Y 的盐溶液中置换出Y;X和Z作原电池电极时,Z为正极;Y和Z的离子共存于电解液中,Y离子先放电;M的离子的氧化性强于Y的离子,则这四种金属的活动性由强到弱的顺序是()
| A.X 〉Y〉Z〉M | B.X 〉Z〉M〉Y |
| C.M 〉Z〉X〉Y | D.X 〉Z〉Y〉M |
某原电池总反应离子方程式为:2Fe3+ +Fe ==3 Fe2+,能实现该反应的原电池是()
A正极为Cu,负极为Fe,电解质溶液为FeCl3溶液
B正极为Cu,负极为Fe,电解质溶液为Fe(NO3)2溶液
C正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液
D正极为Ag,负极为Fe,电解质溶液为CuSO4溶液