下列除杂方法正确的是( )
① 除去乙烷中少量的乙烯:通过酸性高锰酸钾溶液,洗气;
② 除去KNO3中少量的NaCl:溶解,蒸发浓缩,冷却结晶、过滤、干燥;
③ 除去CO2中少量的CO:在空气中点燃;
④ 除去苯中少量的苯酚:加入适量NaOH溶液,分液。
| A.①② | B.②④ | C.③④ | D.②③ |
下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是
| A.H+、NO3-、Fe2+、Na+ | B.K+、Ba2+、OH-、SO42- |
| C.Ag+、NO3-、Cl-、K+ | D.Cu2+、NH4+、Cl-、OH- |
下列关于金属性质的叙述中正确的是
| A.氧气过量时,钠转化为Na2O2 | B.打磨的铝箔加热至熔化时,铝会滴落 |
| C.点燃镁之前,应先用砂纸打磨 | D.铁在纯氧中燃烧生成Fe2O3 |
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
| A.向NaHCO3固体中加入新制的氯水,有无色气泡产生(H+) |
| B.新制氯水使红色布条褪色(HCl) |
| C.将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl-) |
| D.向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,溶液呈红色(Cl2) |
已知下述三个实验均能发生化学反应,下列判断正确的是:
①将铁钉放入硫酸铜溶液中
②向硫酸亚铁溶液中滴入几滴双氧水
③将铜丝放入氯化铁溶液中
| A.实验①中铁钉做氧化剂 | B.实验②中Fe2+具有还原性 |
| C.实验③中发生的是置换反应 | D.上述实验证明氧化性Fe3+>Fe2+>Cu2+ |
在1 L 1 mol·L-1的氨水中,下列说法正确的是
| A.含有1 mol NH3分子 | B.含NH3和NH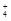 之和为1 mol 之和为1 mol |
| C.含NH3·H2O 1 mol | D.含NH3、NH3·H2O、NH4+之和为1 mol |