用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。
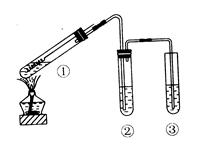 下列实验不合理的是( )
下列实验不合理的是( )
| A.上下移动①中铜丝可控制SO2的量 |
B.②中选用品红溶液验证S O2的生成 O2的生成 |
| C.③中选用NaOH溶液吸收多余的SO2 |
| D.为确认CuSO4生成,向①中加水,观察颜色 |
下列不是元素的电负性应用的是
| A.判断一种元素是金属还是非金属 | B.判断化合物中元素化合价正负 |
| C.判断化学键类型 | D.判断化合物溶解性 |
下列各组中的X和Y两种原子,化学性质一定相似的是
| A.X原子和Y原子最外层都只有一个电子 |
| B.X原子的核外电子排布为1s2,Y原子的核外电子排布为1s22s2 |
| C.X原子2p能级上有三个电子,Y原子的3p能级上有三个电子 |
| D.X原子核外M层上仅有两个电子,Y原子核外N层上仅有两个电子 |
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构
示意图为 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为 下列关系中正确的是
下列关系中正确的是
| A.原子半径:a>c>d>b | B.电负性a>b>d>c |
| C.原子序数:d>a>c>b | D.最高价含氧酸的酸性c>d>a |
已知ClO-、ClO2-、ClO3-、ClO4-微粒中的氯都是以sp3杂化轨道方式成键,其中属于正四面体构型的是
| A.ClO- | B.ClO2- | C.ClO3- | D.ClO4- |
下列说法不正确的是
| A.HCl、HBr、HI的熔、沸点依次升高与分子间作用力大小有关 |
| B.H2O的熔、沸点高于H2S是由于H2O分子之间存在氢键 |
| C.I2易溶于CCl4可以用相似相溶原理解释 |
| D.甲烷可与水形成氢键 |