下列离子方程式正确的是 ( )
A.沸水中滴入FeCl3饱和溶液:Fe3++3H2O Fe(OH)3(胶体)+3H+ Fe(OH)3(胶体)+3H+ |
| B.一小块钠投入水中:Na+2H2O=Na++2OH-+H2↑ |
| C.Ca(HCO3)2溶液中加入足量NaOH溶液:HCO3-+OH-=H2O+CO32- |
| D.Na2CO3溶液中加入醋酸:CO32-+2H+=CO2↑+H2O |
下列说法正确的是()
| A.温度升高水的电离程度增大,pH值增大 |
| B.纯水中c(H+)与c(OH-)的乘积一定等于1×10-14 |
| C.某水溶液中只要c(H+)=c(OH-),则一定是中性的 |
| D.电离程度大的酸一定比电离程度小的酸pH值小 |
a mol FeS与b mol FeO投入到VL、c mol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为()
①(a+b)×63g②(a+b)×189g③(a+b)mol④mol
| A.①④ | B.②④ |
C.②③ | D.①③ |
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为p g/ml,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是()
A. |
B. |
C.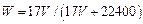 |
D.C="1000Vρ/(17V+22400)" |
第三届中国武陵山区(贵州·铜仁)民族文化节暨2010贵州梵净山文化旅游节在锦江河畔的铜仁民族风情园隆重开幕。在开幕式的晚会中现场观众手持被称为“魔棒”的荧光棒营造了很好的氛围,“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式为:下列说法正确的是()
| A.CPPO属于芳香族化合物 |
| B.CPPO属于高分子化合物 |
| C.1mol CPPO与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4mol NaOH |
| D.1mol CPPO与氢气完全反应,需要氢气10mol |
下列离子方程式正确的是()
| A.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全: Ba2+ + 2OH-+ 2H+ + SO42-= BaSO4↓ + 2H2O |
| B.向100mL 0.1mol/L FeBr2溶液中通入0.01mol的Cl2: 2Fe2+ + 4Br-+ 3Cl2 = 2Fe3+ + 2Br2 + 6Cl- |
| C.AlCl3溶液与过量氨水混合:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| D.向Mg(HCO3)2中加足量的Ca(OH)2溶液: |
Ca2++2OH-+2HCO3-+2Mg2+=CaCO3↓+MgCO3↓+2H2O