下列关于平衡常数的说法正确的是
| A.一定温度下的可逆反应,只有达到平衡时才具有平衡常数 |
| B.化学平衡移动时,平衡常数一定改变 |
| C.对于一个确定的反应来说,平衡常数的数值越大,反应限度越大 |
| D.化学平衡常数大的可逆反应,所有反应物的转化率一定大 |
下列对有关元素的叙述能说明该元素一定是主族元素的是()
| A.原子核外M层有8个电子的元素 |
| B.原子核外L层比M层多一个电子的元素 |
| C.最高价为+7价的元素 |
| D.无负化合价的元素 |
航天飞船可用肼(N2H4)作动力源。已知1g液态肼和足量的液态过氧化氢反应生成N2和水蒸气时放出20.05kJ热量,化学方程式如下:N2H4+2H2O2===N2↑+4H2O。
下列说法中错误的是( )
| A.该反应中肼作还原剂 |
| B.此情况下,液态肼燃烧生成1molN2时放出的热量为641.6kJ |
| C.肼(N2H4)分子中只存在极性共价键 |
| D.该反应的反应物总能量高于生成物的总能量 |
在短周期元素中,原子最外电子层只有1个或2个电子的元素是( )
| A.金属元素 | B.稀有气体元素 |
| C.非金属元素 | D.无法确定为哪一类元素 |
2011年9月,中国女科学家屠呦呦获得被誉为诺贝尔奖“风向标”的拉斯克奖,这是中国医学界迄今为止获得的世界级最高级大奖。她获奖理由是:“因为创制新型抗疟药——青蒿素和双氢蒿素,挽救了全球特别是发展中国家的数百万人的生命。”已知结构如右图所示,则下列说法正确的是 ( )
| A.青蒿素与维生素C一样易溶于水 |
| B.青蒿素的晶体为分子晶体,其化学式为C16H20O5 |
| C.青蒿素不能与NaOH溶液反应 |
| D.青蒿素中含有过氧键,一定条件下有氧化性 |
下列化学反应的产物中,存在同分异构体的是( )
| A.CH3CH2CH2Br在碱性溶液中水解 |
| B.甲苯在催化剂作用下与Cl2发生取代反应 |
C.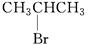 与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 |
D.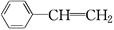 在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |