用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁,如下图所示,将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是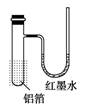
| A.实验中发生的反应都是氧化还原反应 |
| B.铝是一种较活泼的金属 |
| C.铝与氧气反应放出大量的热量 |
| D.铝片上生成的白毛是氧化铝和氧化汞的混合物 |
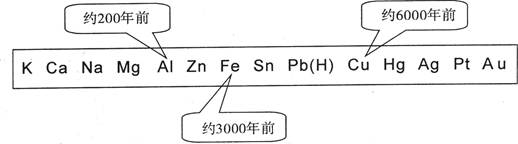
| A.金属的化合价高低 | B.金属的活动性大小 |
| C.金属的导电性强弱 | D.金属在地壳中的含量多少 |
| A.温室效应——二氧化碳 | B.光化学污染——二氧化氮 |
| C.酸雨——二氧化碳 | D.臭氧层破坏——氟氯烃 |

 将一定量A、B装入容积为1L的恒温密闭容器中,发生反应:2A(g)+bB(g)
将一定量A、B装入容积为1L的恒温密闭容器中,发生反应:2A(g)+bB(g) cC(g),1min时达到平衡,C的浓度为xmol·L—1。若保持温度不变,将密闭容器的容积压缩为原来的
cC(g),1min时达到平衡,C的浓度为xmol·L—1。若保持温度不变,将密闭容器的容积压缩为原来的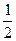 ,重新达到平衡后,C的浓度为2.5x mol·L—1,下列说法正确的是()
,重新达到平衡后,C的浓度为2.5x mol·L—1,下列说法正确的是()
A.化学计量数的关系:b<c
B.容器的容积减小后,该反应的逆反应速率减小
C.原容器中用B的浓度变化表示该反应在1min内的速率为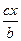 mol·L—1·min—1
mol·L—1·min—1
D.若保持温度和容器的容积不变,充入氦气(不参与反应),平衡不发生移动
在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是()
① K+、Cl-、NO3-、S2-② K+、Fe2+、I-、SO42-③ Na+、Cl-、NO3-、SO42-
④ Na+、Ca2+、Cl-、HCO3-⑤ K+、Ba2+、Cl-、NO3-
| A.①③ | B.③⑤ | C.③④ | D.②⑤ |
某化学科研小组研究在其他条件不变时,改变某一条
件对A2(g)+3B2(g)  2AB3(g)化学平衡状态的影响,
2AB3(g)化学平衡状态的影响,
得到如下图所示的变化规律(图中T表示温度,n表
示物质的量),根据如图可得出的判断结论正确的是
()
A.正反应一定是放热反应
B.达到平衡时A2的转化率大小为:b>a>c
C.若T2>T1,则正反应一定是放热反应
D.b点时,平衡体系中A、B原子数之比接近1:3