某高分子化合物的部分结构如下: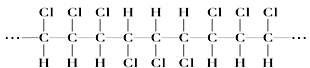
下列说法不正确的是
A.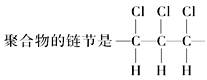 |
| B.聚合物的分子式为(C2H2Cl2)n |
| C.聚合物的单体是CHCl==CHCl |
| D.若n为聚合度,则其相对分子质量为97n |
下列关于乙烯和聚乙烯的叙述中正确的是( )
| A.二者都能使溴水褪色,性质相似 |
| B.二者互为同系物 |
| C.二者最简式相同 |
| D.二者分子组成相同 |
下列有关高分子化合物的叙述中正确的是( )
| A.高分子化合物的特点之一是组成元素简单、结构复杂、相对分子质量大 |
| B.高分子链之间靠分子间作用力结合,因此分子间作用弱,高分子材料强度较小 |
| C.高分子均为长链状分子 |
| D.高分子物质均为混合物 |
苯丙氨酸( )有多种同分异构体。其中同时符合下列两个条件:①有带两个取代基的苯环;②有一个硝基直接连接在苯环上的异构体有( )
)有多种同分异构体。其中同时符合下列两个条件:①有带两个取代基的苯环;②有一个硝基直接连接在苯环上的异构体有( )
| A.3种 | B.5种 | C.6种 | D.10种 |
以下各种模型图都由C、H、O、N中的一种或多种元素构成。下列说法正确的是( )
A.图①是球棍模型,其化学式为:C3H7O2N,是一种蛋白质
B.图②是比例模型,其化学式为:C9H13NO,该物质既能与盐酸反应,又能与氢氧化钠溶液反应
C.图③是球棍模型,其化学式为:C9H10O3,1 mol该物质能消耗3 mol氢氧化钠
D.图③是比例模型,其化学式为:C9H13ON,能够发生消去反应
下列说法不正确的是( )
| A.麦芽糖及其水解产物均能发生银镜反应 |
| B.用溴水即可鉴别苯酚溶液、2,4己二烯和甲苯 |
| C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
D.用甘氨酸( )和丙氨酸( )和丙氨酸(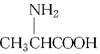 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |