下列化学实验事实解释正确的是
| A.过量的铜屑与稀硝酸作用,反应停止后,再加入1mol/L稀硫酸,铜屑又逐渐溶解,是因为铜可直接与1mol/L稀硫酸反应 |
| B.铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面形成了一层致密稳定的氧化膜 |
| C.相同物质的量浓度乙酸铅溶液导电能力比乙酸钙弱得多,说明乙酸铅属于非电解质 |
| D.浓NH4Cl溶液处理过的舞台幕布不易着火,是因为处理后幕布质量增加,着火点升高 |
铜粉放入稀硫酸溶液中,加热后无明显现象发生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出。该盐是
| A.Fe2(SO4)3 | B.Na2CO3 | C.KNO3 | D.FeSO4 |
X、Y、Z、W均为短周期元素,它们在周期表中的位置如下图所示。若X原子的最外层电子数比其次外层电子数多3个,下列说法不正确的是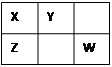
| A.原子半径:Z>X>Y |
| B.最高价氧化物对应水化物的酸性:Z>W |
| C.W的单质是制取盐酸的原料之一 |
| D.X、W的氢化物相遇会产生白烟 |
将等物质的量的SO2和Cl2混合后通入含有品红和Ba(NO3)2的混合溶液里,发生的现象是
①溶液很快褪色 ②溶液不褪色 ③有沉淀生成 ④溶液仍然透明
| A.仅①和④ | B.仅①和③ | C.仅②和③ | D.仅②和④ |
下列电子式正确的是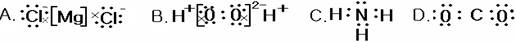
a、b、c三种元素的原子序数均小于20,a、b两元素的阳离子和c元素的阴离子都有相同的电子层结构,a原子的半径大于b原子的半径,则三种元素的原子序数的关系是
| A.a>b>c | B.b>a>c | C.c>b>a | D.a>c>b |