下列反应的离子方程式正确的是 ( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体: |
| B.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
C.实验室用浓盐酸与MnO2反应制Cl2: |
| D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
反应X(g)+Y(g) 2Z(g);
2Z(g); H<0,达到平衡时,下列说法正确的是
H<0,达到平衡时,下列说法正确的是
| A.降低温度,能使Y的转化率增大 |
| B.加入催化剂,能使Z的产率增大 |
| C.增大c(X),X的转化率增大 |
| D.缩小容器体积,平衡向右移动 |
下列有关说法正确的是
| A.将AlCl3溶液蒸干得到的固体是AlCl3 |
| B.锅炉水垢中的CaSO4可用饱和Na2CO3溶液浸泡,再用稀盐酸溶解除去 |
| C.加热纯水,KW变大、pH变小、呈酸性 |
| D.在饱和BaSO4溶液中加入少量Na2SO4固体,溶液中c(Ba2+)增大 |
室温下,下列各组离子在给定条件的溶液中一定能大量共存的是
| A.由水电离产生的c(H+)=10﹣12 mol•L一1的溶液中:K+、Na+、Fe2+、NO3﹣ |
| B.pH=7的溶液中:Al3+、Cl-、HCO3﹣、SO42﹣ |
| C.pH=13的溶液中:K+、Ba2+、Cl﹣、OH﹣ |
| D.pH=13的溶液中:NH4+、Na+、HS﹣、Cl﹣ |
可逆反应2NO2(g)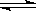 N2O4(g) △H<0,在密闭容器中进行并达到平衡,欲通过改变条件达到新平衡后使混合气体颜色加深,可采取的措施是
N2O4(g) △H<0,在密闭容器中进行并达到平衡,欲通过改变条件达到新平衡后使混合气体颜色加深,可采取的措施是
| A.增大容器体积 |
| B.保持温度压强不变,充入N2O4(g) |
| C.保持温度压强不变,充入NO2(g) |
| D.保持容器容积不变,升高温度 |
某学生的实验报告所列出的下列数据中合理的是
| A.用25mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70mL |
| B.用托盘天平称得25.20g NaCl |
| C.用广泛pH试纸测得某溶液的pH为2.3 |
| D.用10mL量筒量取7.13mL稀盐酸 |