下列叙述中,正确的是 ( )
| A.Na比K的金属性强 | B.Na和K的电子层数相同 |
| C.Na和K都是强还原剂 | D.Na和K灼烧时都能使火焰呈现紫色 |
已知CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-Q1①
2H2(g)+O2(g)===2H2O(g)ΔH=-Q2②
H2O(g)===H2O(l) ΔH=-Q3③
常温下,取体积比为4∶1的甲烷和H2的混合气体112 L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为( )
| A.4Q1+0.5Q2 | B.4Q1+Q2+10Q3 | C.4Q1+2Q2 | D.4Q1+0.5Q2+9Q3 |
某温度下,反应SO2(g)+  O2(g)
O2(g)  SO3 (g) 的平衡常数K1=50,在同一温度下,反应2SO3(g)
SO3 (g) 的平衡常数K1=50,在同一温度下,反应2SO3(g)  2SO2(g) + O2(g)的平衡常数K2的值为( )
2SO2(g) + O2(g)的平衡常数K2的值为( )
| A.2500 | B.100 | C.4×10-4 | D.2×10-2 |
在一个固定体积的密闭容器中,放入3L X(气)和2L Y(气),在一定条件下发生下列反应 4 X (g) + 3 Y(g) 2 Q(g) + n R(g),达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小33.3%,则该反应方程式的n值是( )
2 Q(g) + n R(g),达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小33.3%,则该反应方程式的n值是( )
A 6 B 5 C 4 D 3
在密闭容器中进行下列反应:M(g) + N(g)  R(g) + 2L此反应符合右图,下列叙述正确的是
R(g) + 2L此反应符合右图,下列叙述正确的是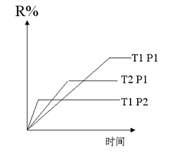
| A.正反应吸热,L是气体 | B.正反应吸热, L是固体 |
| C.正反应放热,L是气体 | D.正反应放热,L是固体或液体 |
在一个固定体积的密闭容器中,2molA和1molB发生反应2A(g)+ B(g)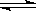 3C(g)+D(g),达到平衡时,C的浓度为W mol/L。维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为W mol/L,该配比是()
3C(g)+D(g),达到平衡时,C的浓度为W mol/L。维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为W mol/L,该配比是()
| A.3molC+1molB | B.1molA+0.5molB+1.5molC+0.5molD |
| C.4molA+2molB | D.3molC+1molD+2molA+1molB |