设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是
| A.1mol NH3所含有的原子数为NA |
| B.常温常压下,22。4L氧气所含的原子数为2NA |
| C.常温常压下,48g O3所含的氧原子数为3NA |
| D.1 L 0.1mol/LNaCL溶液中所含的Na+为Na |
在给定的溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有()
| A.所含溶质有Na2SO4的溶液:K+、AlO2-、NO3-、Al3+ |
| B.pH值为1的溶液:Cu2+、Na+、Mg2+、NO3- |
| C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| D.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I- |
下列事实不能用勒夏特列原理解释的是 ()
| A.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| B.高压比常压有利于合成SO3的反应 |
| C.红棕色的NO2,加压后颜色先变深后变浅 |
| D.黄绿色的氯水光照后颜色变浅 |
下列关于判断过程的方向的说法正确的是()
| A.所有自发进行的化学反应都是放热反应 |
| B.由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程 |
| C.高温高压下可以使石墨转化为金刚石是自发的化学反应 |
| D.同一物质的固、液、气三种状态的熵值相同 |
下列方程式书写正确的是()
A.NaHCO3在水溶液中的电离方程式:NaHCO3 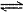 Na++HCO3- Na++HCO3- |
B.H2SO3的电离方程式H2SO3 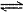 2H++SO32- 2H++SO32- |
C.CO32-的水解方程式:CO32-+2H2O  H2CO3+2OH- H2CO3+2OH- |
D.HS-的水解方程式:HS-+H2O  H2S+OH- H2S+OH- |
在恒温恒容的密闭容器中,对于可逆反应A(g)+B(g) 2C(g),可以判断达到化学平衡状态的是( )
2C(g),可以判断达到化学平衡状态的是( )
| A.体系压强不变 | B.单位时间消耗n molA,同时生成2nmolC |
| C.A的转化率不变 | D.容器内气体密度不变 |