下列离子方程式正确的是 ( )
| A.高锰酸钾与浓盐酸反应:2 MnO4- + 10 Cl- + 16 H+ =" 2" Mn2+ + 5 Cl2↑ + 8 H2O |
| B.标准状况112 mLCl2通入10 mL 1mol/LFeBr2溶液:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
C.浓盐酸和KClO3反应: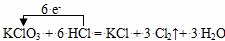 |
| D.硫化钠溶于水显碱性:S2- + 2H2O = H2S + 2OH- |
TBC是优良的增塑剂,具有很好的相容性,且挥发性小、耐寒、耐光及耐水等,广泛用于医学卫生用品,它的结构式如右图,合成时柠檬酸与正丁醇合成数据如下:

下表中实验数据均为用活性炭固体杂多酸作催化剂,实验时催化剂总量占原料的1%,实验结果如下表。表1:酸醇物质的量之比对酯化率的影响;表2:酯化时间对酯化率的影响;表3:酯化率随温度变化情况。
| 表1 |
n(酸)︰n(醇) |
1︰5.0 |
1︰5.5 |
1︰6.0 |
1︰6.5 |
1︰7.0 |
| 酯化率/% |
95.1 |
96.3 |
97.0 |
97.4 |
97.2 |
|
| 表2 |
时间/h |
0.5 |
1.0 |
2.0 |
3.0 |
5.0 |
| 酯化率/% |
40.0 |
70.2 |
94.3 |
97.4 |
97.4 |
|
| 表3 |
温度/℃ |
130 |
140 |
145 |
150 |
160 |
| 酯化率/% |
89.5 |
96.2 |
97.4 |
97.4 |
97.2 |
试回答下列问题
(1)酯化反应适宜的条件n(酸)∶(醇)、时间/h、温度/℃分别是:▲(选填序号)。
A.1∶5,1,130 B.1∶5.5 ,1,140
C.1∶7 ,2,160 D.1∶6.5 ,3,145
(2)TBC的一种标准谱图如右,它是 ▲(A、1H-NMR图谱 B、红外光谱 C、质谱)
(3)TBC与足量NaOH溶液反应的化学方程式:▲。
(4)柠檬酸的一种同分异构体A,能发生如下转化:
A可能的结构式为:▲(只写一种)。
X、Y、Z、W有如右图所示的转化关系,已知焓变:
△H=△H1+△H2,则X、Y可能是
①C , CO②AlCl3, Al(OH)3③Fe , Fe(NO3)2 ④FeBr2, FeBr3
| A.①②③④ | B.①② | C.③④ | D.①②③ |
自来水加工处理流程如下,下列有关说法不正确的是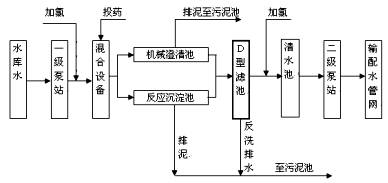
| A.若用FeSO4作混凝剂,最终铁将以Fe(OH)2形式进入反应沉淀池 |
| B.投药时常加入适量的石灰,是为了除去水中Mg2+、HCO3-等 |
| C.自来水生产中,前加氯起消毒杀菌作用,后加氯是保持水中有效氯的含量,防止自来水二次污染 |
| D.用ClO2消毒自来水,消毒效率是同质量氯气的2.63倍 |
下列离子方程式不正确的是
A.用两个铜电极电解食盐水:2Cl-+2H2O  2OH- + H2↑+ Cl2↑ 2OH- + H2↑+ Cl2↑ |
| B.AgCl悬浊液中加入硫化钠饱和溶液:2AgCl + S2-=Ag2S +2Cl- |
| C.Ca(HCO3)2溶液中加入过量KOH溶液:Ca2+ + HCO3- +OH- =CaCO3↓+ H2O |
| D.Fe(OH)3溶于过量的HI溶液:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
| A.2.24LCl2中含有的原子数一定为0.2 ×6.02×1023 |
| B.0.1L2mol·L-1的Na2CO3溶液中含有的CO32-数目为0.2 ×6.02×1023 |
| C.0.88gC3H8中含有的共价键总数目为0.2 ×6.02×1023 |
| D.7.8g过氧化钠粉末与水反应转移的电子数为0.2 ×6.02×1023 |