质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为
| A.大于2c mol/L | B.等于2c mol/L |
| C.小于2c mol/L | D.在c mol/L—2c mol/L之间 |
化学与生产、生活密切相关,下列有关说法不正确的是
| A.使用含有氯化钠的融雪剂会加快桥梁的腐蚀 |
| B.可溶性铜盐有毒,故人体内不存在铜元素 |
| C.在海轮外壳装上锌块,可减缓船体的腐蚀速率 |
| D.中秋佳节月饼中用小袋包装的铁粉来防止月饼氧化变质 |
食品干燥剂应无毒、无味、无腐蚀性及环境友好。下列说法错误的是
| A.硅胶可用作食品干燥剂 |
| B.P2O5不可用作食品干燥剂 |
| C.六水合氯化钙可用作食品干燥剂 |
| D.加工后具有吸水性的植物纤维可用作食品干燥剂 |
海水开发利用的部分过程如图所示。下列说法错误的是
| A.向苦卤中通入Cl2是为了提取溴 |
| B.粗盐可采用除杂和重结晶等过程提纯 |
| C.工业生产中常选用NaOH作为沉淀剂 |
| D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收 |
给定条件下,下列选项中所示的物质间转化均能一步实现的是
A.粗硅 SiCl4 SiCl4 Si Si |
B.Mg(OH)2 MgCl2(aq) MgCl2(aq) 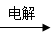 Mg Mg |
C.Fe2O3 FeCl3(aq) FeCl3(aq)  无水FeCl3 无水FeCl3 |
D.AgNO3(aq) 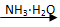 [Ag(NH3)2]OH(aq) [Ag(NH3)2]OH(aq)  Ag Ag |
在通风橱中进行下列实验:
| 步骤 |
 |
 |
|
| 现象 |
Fe表面产生大量无色气泡,液面上方变为红棕色 |
Fe表面产生少量红棕色气泡后,迅速停止 |
Fe、Cu接触后,其表面产生红棕色气泡 |
下列说法中不正确的是
A.Ⅰ种气体有无色变红棕色的化学方程式为:2NO+O2=2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化