将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是( )
| A.做该实验时环境温度为22℃ |
| B.该实验表明化学能可以转化为热能 |
| C.NaOH溶液的浓度约为1.0 mol/L |
| D.该实验表明有水生成的反应都是放热反应 |
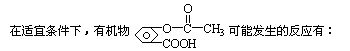 ①水解 ②加成 ③酯化 ④消去 ⑤银镜 ⑥中和。下列选项正确的()
①水解 ②加成 ③酯化 ④消去 ⑤银镜 ⑥中和。下列选项正确的()
| A.①②③⑥ | B.③④⑤⑥ | C.只有②④ | D.只有③⑥ |
某烃W与Br2的加成产物是2,2,3,3—四溴丁烷,与W属于同系物的是
| A.乙炔 | B.2—丁烯 | C.1,3—丁二烯 | D.异戊二烯 |
 ()
()
| A.3种 | B.4种 | C.5种 | D.6种 |
银锌电池的充电和放电过程可表示为: 2Ag+Zn(OH)2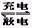 Ag2O+Zn+2H2O,此电池放电时,负极上发生反应的物质是( )
Ag2O+Zn+2H2O,此电池放电时,负极上发生反应的物质是( )
| A.Ag | B.Zn(OH)2 | C.Ag2O | D.Zn |
有关金属腐蚀的论述,正确的是().
| A.金属的腐蚀一定伴有电流产生 |
| B.Fe在干燥的氯气里比在潮湿的空气里更易被腐蚀 |
| C.发生化学能转变为电能的腐蚀时较活泼的金属总是作正极而被腐蚀 |
| D.发生电化腐蚀时都有能量的转变,且被腐蚀的金属总是失电子 |