现代无机化学对硫氮化合物的研究是最为活跃的领域之一。如图是已经合成的最著名的硫氮化合物的分子结构。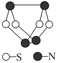
下列说法正确的是( )
| A.该物质的分子式为SN |
| B.该物质的分子中所有原子的最外层都达到8电子稳定结构 |
| C.含有1 mol的该物质的微粒中含有共价键为8NA |
| D.该物质与化合物S2N2互为同位素 |
对于反应N2+3H2 2NH3(正反应为放热反应),能使正反应速率和逆反应速率增大的因素有:①升高温度、②使用催化剂、③增大压强、④增加N2或和H2的浓度
2NH3(正反应为放热反应),能使正反应速率和逆反应速率增大的因素有:①升高温度、②使用催化剂、③增大压强、④增加N2或和H2的浓度
| A.①②③ | B.②③④ | C.①②③④ | D.①③④ |
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积, ③溶液的温度,④氯离子的浓度,影响反应速率的因素是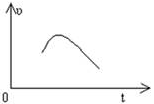
| A.①④ | B.③④ | C.②③ | D.①②③ |
下列说法正确的是
| A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大单位体积内活化分子的数目,有效碰撞次数增大,化学反应速率增大 |
| C.升高温度能使化学反应速率增大,唯一的原因是增加了反应物分子中活化分子的百分数 |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
下列措施肯定能使化学平衡移动的是
| A.增大反应物的量 | B.增加压强 | C.升高温度 | D.使用催化剂 |
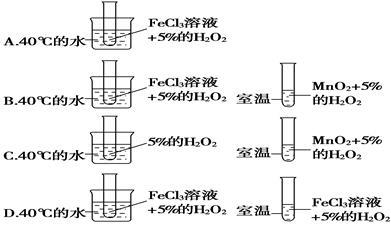
已知FeCl3和MnO2都可作H2O2分解制O2的催化剂,为了探究温度对化学反应速率的影响,下列实验方案可行的是